蛋白质/多肽液相分析中的流动相选择
有机溶剂可将吸附在疏水界面的蛋白质洗脱(图14)。
在梯度洗脱期间,当有机溶剂量达到针对每一蛋白质的特定浓度时,蛋白质就会从疏水界面上解吸,继续顺着柱向下,从而从柱中洗脱。
图14. 当有机改性剂的浓度达到特定值时,蛋白质从疏水界面洗脱。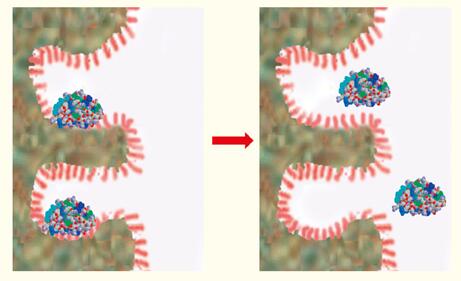
乙腈。在多肽的反相色谱分离时Z常用的有机溶剂为乙腈。为什么选择乙腈?
乙腈易挥发,易从样品中去除。
乙腈黏度低,柱压低。
乙腈的紫外吸收截止波长较短。
乙腈长期用于分离应用。
异丙醇。异丙醇在多肽的色谱分离中具有重要作用。尽管异丙醇黏度大(会增大柱压),很少单独用作有机改性剂,但其在提高一些多肽的回收率方面具有重要作用,尤其是强疏水性蛋白。
在此类情况下,以1%~5%的恒定浓度加入异丙醇,以提高疏水性多肽的回收率或洗脱。
其它有机改性剂。很少使用甲醇或乙醇等有机改性剂,除非在分离强疏水性蛋白时。此外,由于乙醇毒性低,因此还用于蛋白质的大规模纯化。
梯度洗脱。多肽的洗脱几乎都采用梯度洗脱法,采用梯度洗脱法分离时,逐渐增大有机溶剂的相对浓度。
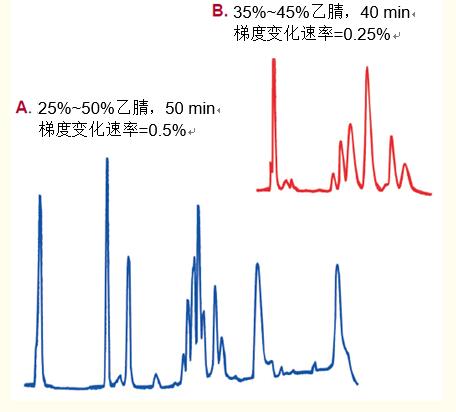
当有机改性剂的浓度升到解吸所需的特定浓度时,蛋白质和多肽就从柱上洗脱。如图15所示,有机改性剂的浓度(梯度)变化速率越慢,这些蛋白亚基的分辨率越高。
在该例中,相较于每分钟0.5%的梯度变化速率,每分钟0.25%的梯度变化显着提高了分辨率。
蛋白质/多肽的保留机制的图1中显示了采用每分钟0.15%的梯度变化速率时几种胰岛素的分离过程。采用每分钟0.05%的梯度变化速率洗脱时,分辨率Z大。
图15. 一般情况下,降低有机溶剂浓度变化速率会提高分辨率。
A. 细胞色素c亚基
B. 色谱图A中间片段的重现。
色谱柱:C4 宽孔柱, 4.6 x 250 毫米
降低梯度变化速率增加分辨率时,所需的分析时间必须尽可能短。
但是,梯度变化速率的调整在优化蛋白质和多肽的分辨率方面非常重要。
有时,降低梯度变化速率时,多肽会表现出特异行为(图16)。
分辨率有时不会按照预期增加,反而会降低,导致出现共洗脱,甚至洗脱顺序也会颠倒。
在图16的示例中,洗脱时间为45分钟时多肽11和12表现出Z佳的分离效果。
当洗脱时间增加至90分钟时,多肽11和12间的分辨率降低;而当洗脱时间增加至160分钟时,出现共洗脱峰。
这种保留行为是多肽表面相互作用的结果,导致这种行为的原因目前尚不清楚。
因此,在进行多肽分离时,尤其是在分离蛋白酶水解物时,观察分辨率随梯度坡度降低的变化很重要。
如果分辨率未增加,反而降低,则必须优化梯度变化速率,以Z大化整体分辨率。
图16. 多肽间分辨率有时随着溶剂浓度变化速率的降低(洗脱时间增加)而降低。
这将导致分辨率降低或共洗脱峰的出现,如人生长激素肽图中多肽11和12例示。
在一些情况下,多肽甚至会逆转洗脱顺序。
样品人生长激素的胰蛋白酶水解物。部分显示了多肽图谱。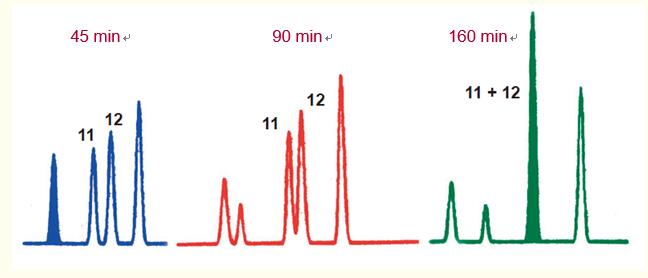
色谱柱:C18宽孔柱,4.6 x 150 mm
洗脱液:梯度:0~60%乙腈与水溶性溶剂和0.1%TFA混合液和有机溶剂与0.08%TFA混合液在一定时间内形成梯度洗脱。
蛋白质和多肽的反相色谱分析法需要“离子对试剂”。
在流动相中加入离子对试剂,以实现良好的峰形。
目前认为,在没有离子对试剂的情况下,硅胶表面的金属杂质是导致蛋白质/多肽峰形较差的原因。
三氟乙酸。三氟乙酸(TFA)是Z常用的离子对试剂。将浓度为~0.1%的三氟乙酸加入流动相,会在大多数柱上产生良好的峰形(图17)。
降低TFA的浓度能提高LC-MS的检测灵敏度(见22~25页),但由于硅胶表面存在杂质,可能会导致硅胶柱上的峰形较差。
但采用高纯度硅胶柱时,可加入低浓度TFA(图17A——0.01% TFA)。
图17. TFA浓度对峰形和选择性的影响
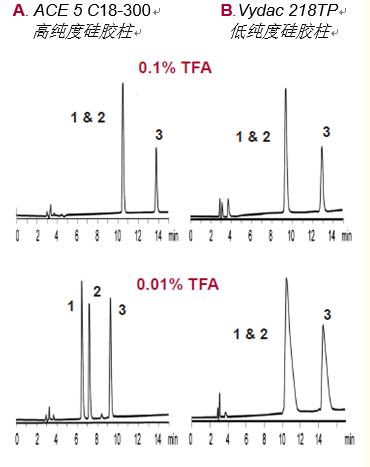
洗脱液:加入如图所示的TFA,以20%~32%的乙腈(ACN)梯度洗脱,洗脱时间为15分钟。
样品1.血管紧张素II 2.血管紧张素III3.血管紧张素I
其它离子对试剂。尽管目前为止TFA仍是Z常用的离子对试剂,但蛋白质/多肽分离有时会采用磷酸和七氟丁酸(HFBA)等其它试剂。
如图18所示,一些情况下,磷酸可分离一些TFA无法分离的多肽。通常磷酸盐使用浓度约为20-30 mM,pH为2~2.5。此外,磷酸盐缓冲液对一些蛋白质的分离效果要优于TFA。
尽管同TFA一样,磷酸盐缓冲液使用的pH通常较低,但磷酸盐缓冲液也能适应较高的pH,为选择性和分辨率的改变提供了机会(见17页)。
将磷酸盐作为离子对试剂的主要弊端是:磷酸盐不挥发,很难从肽中去除。
一些时候,七氟丁酸用作组蛋白等碱性蛋白分离的离子对试剂
图18. 使用除TFA以外的离子对试剂可能会产生不同的选择性
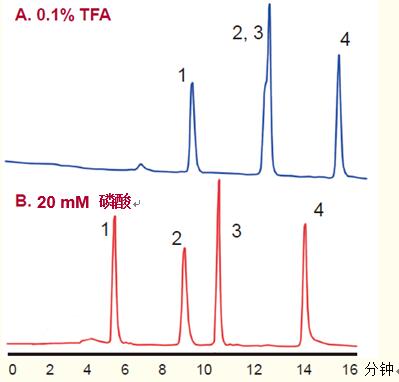
条件
色谱柱:C18 宽孔柱, 4.6 x 250 毫米
洗脱液:
A.4%~40% 乙腈—0.1%TFA体系,pH=2,18分钟梯度洗脱。
B.4%~40% 乙腈—20mM 磷酸体系,pH=2,18分钟梯度洗脱。
样品:
缓激肽
神经降压素
蛙皮素
章鱼唾腺精
pH值对多肽保留行为的影响。不论采用TFA和磷酸,还是其它离子对试剂,用于多肽分离的反相流动相通常适应的pH值较低。
在低pH值条件下,羧酸基团——端羧基,以及天冬氨酸和谷氨酸的侧链会进行质子化,且仅有轻微极性。
将流动相的pH值增加至6~7将会使羧酸基团离子化,减弱多肽的疏水性。这将降低各种多肽的保留值,但尤其影响含天冬氨酸或谷氨酸的多肽(图19)。
与其它多肽相比,含天冬氨酸和谷氨酸的多肽的保留值降低更多,从而改变了选择性。尽管增加多肽分离流动相pH的做法不经常采用,但它可以在一些特定情况下发挥作用。
图19. 流动相的pH值会影响多肽的保留值,尤其是含酸性氨基酸残基(天冬氨酸和谷氨酸)的多肽。
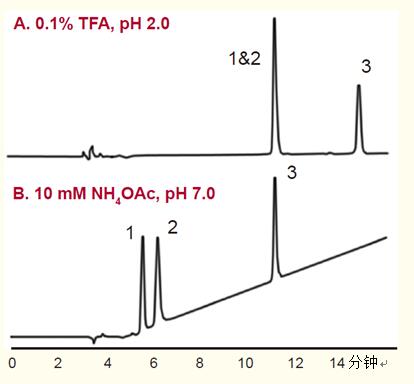
条件
色谱柱:ACE 5 C18-300,4.6 x 250 mm
洗脱液:
A.20%~32% 乙腈—0.1%TFA体系,pH=2,15分钟梯度洗脱。
B.20%~32% 乙腈—10mM NH4OAc体系,pH=7,15分钟梯度洗脱。
样品
血管紧张素II
血管紧张素III
血管紧张素I
流速。流动相的流速对反相GX液相色谱法分离的分辨率影响不大。
如图20所示,流动相流速为0.5、1.0或2.0 ml/min时,胰蛋白酶图谱中多肽的分辨率大致相同。
但梯度体积必须恒定才能维持分辨率一致。
这需要随着流速的增加减少梯度洗脱时间。
体系压力随着流速的增加而增加;体系压力可能会限制可用的流速。
此外,较高的流速还会使检测灵敏度稍有降低,但可能增加大分子蛋白或疏水性蛋白的溶解度。
图20. 流动相的流速对多肽的分辨率影响不大。随着流速的变化,总梯度体积必须保持恒定才能维持分辨率一致。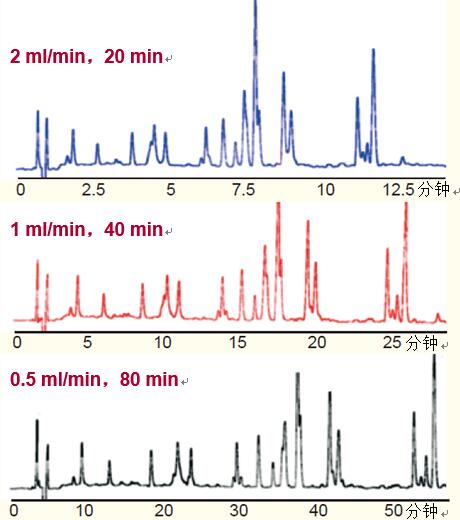
条件
色谱柱:C18小孔柱,4.6 x 250 mm
洗脱液:10%~50% 乙腈~0.1% TFA 体系,时间、流速如图所示
样品β-乳球蛋白的胰蛋白酶水解物

 评论
评论