
身处战“疫”时期,大家的注意力都集中在肆虐的新型冠状病毒感染肺炎上。同舟共济,同心战“疫”!
与此同时,一年一期的微生物药敏领域圣经——CLSI M100的年度更新如期发布了。那今年CLSI又有哪些重大更新,我们又可以从中学习到哪些新的知识呢?
有没有新增药物?
现有药物有没有折点变更?
命名、分类等方面有没有相关更新?
梅里埃将为大家提炼和解读2020年M100文件的主要更新要点,请听本文一一道来。
01 更新汇总方面
拿到CLSI的diyi时间,根据以往的习惯,我们都是直接翻到更新汇总,看一下有什么主要更新。此次的更新汇总给了我们一个惊喜,更新版使用表格方式进行阐述,更为清晰明了。
图例 CLSI M100 ED 30中更新汇总图解

且新版文件在更新汇总中列举了每一处更新所处的页码,这样就为我们diyi时间了解到今年CLSI的Z新更新提供了极大的便利。(本文的编写也因此方便了不少)
02 黏菌素与多粘菌素B药敏方面的更新
在今年黏菌素与多粘菌素B有了多条相关更新。包括更新了黏菌素和多粘菌素B对于肠杆菌目细菌、铜绿假单胞菌和不动杆菌的折点,并对此增加了解释;考虑到目前尚无商品化系统通过FDA的认证,普通实验室无法常规开展肉汤微量稀释法的测试,为此提供了粘菌素方面2个可选替代试验 -- CAT黏菌素琼脂试验和CBDE黏菌素肉汤纸片洗脱试验。
1.多粘菌素类KJ药物折点方面的更新
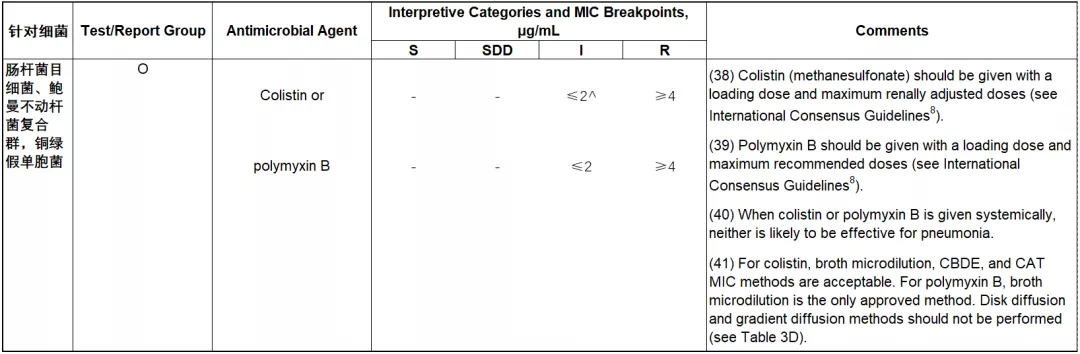
*仅肠杆菌目细菌 中介折点之后有^标记
通过折点表格,发现除了增加了折点以外,同时增加了4条相关备注。通过阅读备注,我们发现多粘菌素类药物的药敏测试和报告有这样一些要点:
目前多粘菌素类药物仅有中介和耐药折点,而没有敏感折点,结合其后的注解(38),(39)来看,在使用黏菌素和多粘菌素B时,需要给予负荷剂量,并根据肾功能给予Z大剂量进行ZL。因此黏菌素和多粘菌素B在报告时只有2种结果解释方式,MIC≤2时报告为中介,MIC≥4时报告为耐药,且建议加上相关备注。
关于黏菌素和多粘菌素B使用剂量的具体问题,CLSI推荐了一篇国际共识供大家参考:Tsuji BT, Pogue JM, Zavaxcki AP等人发表于19年Pharmacotherapy. 2019;39(1):10-39.上的多粘菌素类药物国际共识[1]。此共识为ACC,IDSA ,ESCMID ,SCCM ,SIDP 的共同共识,有必要进行学习。
注解(40)条强调:对于肺炎,即使黏菌素或多粘菌素B全身给药,亦很可能无效,因此在报告呼吸道相关标本时建议加上此条注解。
此外关于药敏方面,CLSI仍然强调目前对于多粘菌素B唯yi的药敏方法仍为肉汤微量稀释法,而黏菌素除了肉汤微量稀释法以外,还可以选择CAT黏菌素琼脂试验和CBDE黏菌素肉汤纸片洗脱试验。这2种方法的具体操作方法和结果解读,可见下文。
2. CAT 黏菌素琼脂试验介绍
CAT 黏菌素琼脂试验需要3块分别含有1 μg/mL、2 μg/mL和4 μg/mL黏菌素的琼脂平板以及一块不含黏菌素的琼脂平板,一次Z多可测试10株菌株,目前此方法仅适用于肠杆菌目细菌以及铜绿假单胞菌。具体流程如下:
接种菌悬液:将待测菌使用生理盐水配置成0.5麦氏菌悬液,而后再使用生理盐水进行10倍稀释;
将平板进行区块划分,一块平板Z多可以划分10个区块,进行10个测试,如下图1;
以移液器或10µL接种环,取10µL上述第1步配置的稀释后菌悬液,接种平板合适区域;
同时接种10µL接种血平板,确认菌悬液为纯培养;
上述平板33-35℃培养,空气环境下培养16-20小时;
读取结果:
确认血平板为纯培养
检查生长对照琼脂平板,确认存在融合生长(下图1 A平板),以确认试验有效
使用透射光仔细阅读,检查黏菌素平板上的菌落或薄雾状生长,(即便一个菌落生长也确认为生长)读取完全YZ的Z低浓度为MIC
图1 CAT试验示意图

1#为铜绿假单胞菌 ATCC 27853;
2# 为大肠埃希菌 AR Bank #0349 (mcr-1)
3. CBDE黏菌素肉汤纸片洗脱试验介绍
一次测试的材料需要准备配置封装10ml CAMHB 4支,黏菌素(10µg)纸片7张,具体操作过程如下:
将CAMHB试管(10 mL)和黏菌素纸片恢复至室温,并在4支试管上分别标记1、2、4 µg/mL和生长对照(GC),如下图2;
分别于1µg/mL的试管中加入 1张黏菌素(10µg)纸片;2µg/mL的试管中加入 2张黏菌素(10µg)纸片;4µg/mL的试管中加入 4张黏菌素(10µg)纸片。注意无菌操作;
将已添加纸片的试管轻轻旋涡,保持纸片中的黏菌素在室温洗脱至少30分钟,但不能超过60分钟;
制备接种菌悬液:将待测菌使用生理盐水配置成0.5麦氏菌悬液;
加 50µL菌悬液至上述 4个试管中,使Z终接种浓度约为7.5 × 105 CFU/mL;
使用10µL接种环取菌悬液,接种血平板;
盖紧试管盖,并慢速混合旋涡每一个已接种的试管。建议慢速以防止黏菌素黏附于盖子和凹液面上方的玻璃表面;
进行孵育,孵育前轻轻的松紧盖子,孵育条件为33-35℃培养,空气环境下培养16-20小时;
读取结果:
确认血平板为纯培养
检测生长对照管,必须存在明显浊度才能确认试验有效。注意:某些铜绿假单胞菌可能只在近凹液面处生长
阅读完全YZ受试菌生长的Z低浓度为MIC
图2 CBDE 试验示意图

A 铜绿假单胞菌ATCC 27853 B大肠埃希菌 AR Bank #0349 (mcr-1)
4. 对于这两个试验的优缺点和用途CLSI也进行了分析,具体如下表
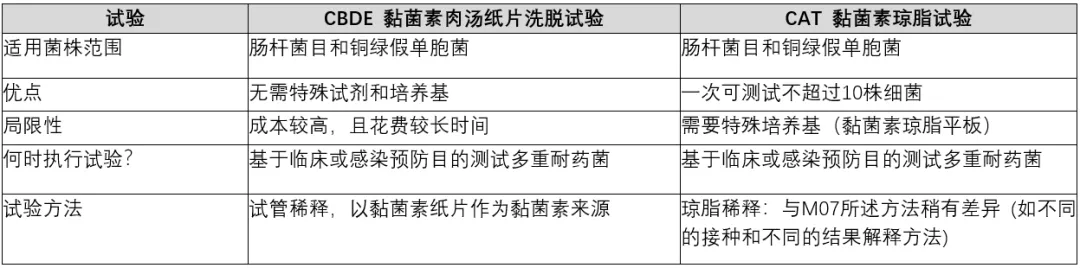
当发生异常情况如高浓度生长,低浓度不生长的情况,需要进行重复试验,如仍存在此种情况,引起原因可能有这样一些:
高浓度试管或平板被污染
异质性耐药
试管/平板中抗生素浓度错误
接种错误
5. QC方法和QC频率
此两种方法同样不是规范化的商品化试剂盒,因此QC非常重要,推荐的可用的质控菌株为大肠埃希菌AR Bank #0349 mcr-1 (≤ 1–4 µg/mL, 靶值2 µg/mL)c 和铜绿假单胞菌ATCC®d 27853(≤ 1–4 µg/mL)。质控频率为,当每周测试超过一次时,可以进行周质控。如果是偶尔进行测试则每次都需要进行质控。
03 分类和命名的更新
大家也可以发现上文中多次出现肠杆菌目这一说法,这是因为CLSI与EUCAST几年均采用了2016年Z新的分类学方法,将肠杆菌科(family Enterobacteriaceae)升级成肠杆菌目(order Enterobacterales)。目前肠杆菌目包括7个科,分别是布杰约维采菌科(Budviciaceae)、肠杆菌科(Enterobacteriaceae), 欧文菌科(Erwiniaceae)、哈夫尼亚菌科(Hafniaceae)、摩根菌科(Morganellaceae)、溶果胶菌科(Pectobacteriaceae)和耶尔森菌科(Yersiniaceae),具体可见下图。
图3 新的肠杆菌目细菌分类图[2]
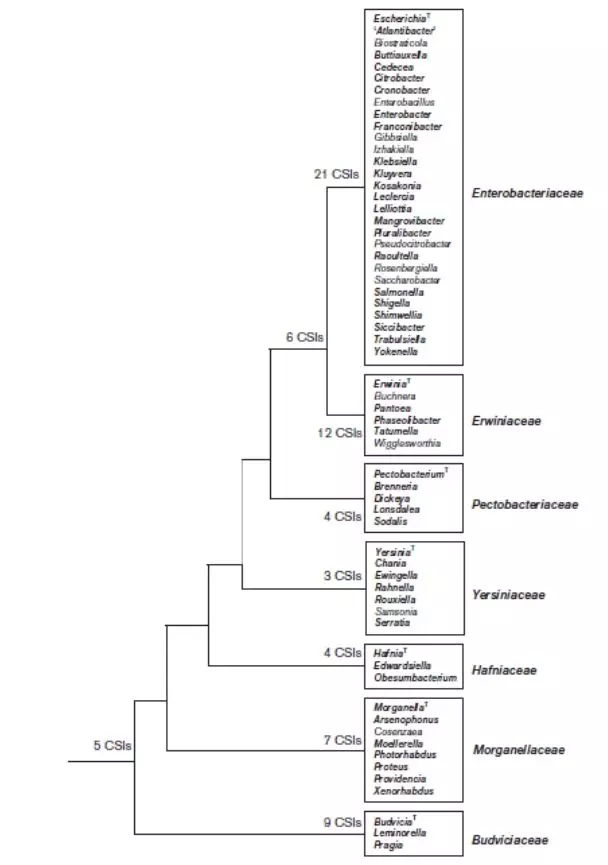
此外伤寒沙门菌(Salmonella Typhi)和副伤寒沙门菌(Salmonella Paratyphi)重新命名为肠沙门菌伤寒血清型(Salmonella enterica ser. Typhi)和肠沙门菌副伤寒血清型(Salmonella enterica ser. Paratyphi),这也是分类学上很早确认的新分类和命名。
此外将“感染控制infection control”变更为“感染预防infection prevention”,这样的定义更为精确。
将MRSA的全名改成了甲氧西林(苯唑西林)耐药的金黄色葡萄球菌,缩写仍不变。
04 中介定义的改变
看药敏表格时,可以发现在中介折点范围后增加了^符号,这是指中介的定义进行了变更,新增了2点解释,带有^的中介表示已知某些药物可在尿液中浓缩以及一些药物可能在其他解剖部位(上皮衬液)潜在浓缩,对于此类药物的中介后面将会加上^符号。此外在sdd和I的解释中也增加了。“该分类亦包含针对测试方法固有变异的一个缓冲区,以防止微小的、未受控制的技术因素导致较大的错误结果,特别是对那些药物毒性范围窄的药物”的说法。
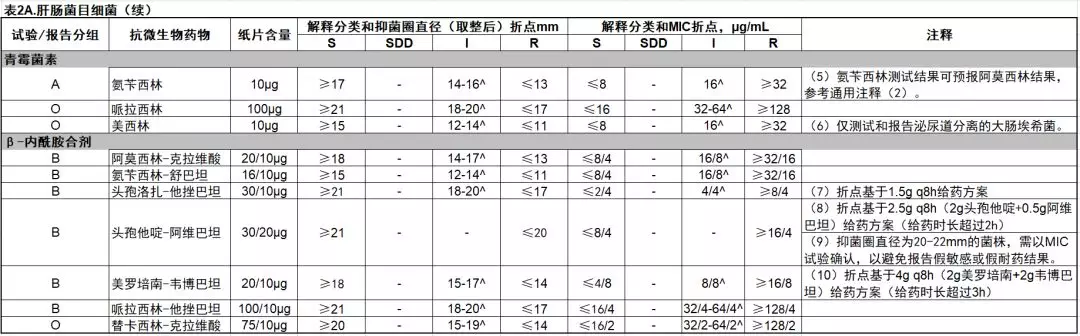
目前此类中介,主要集中于表格2A的肠杆菌目药敏表格及2B-1的铜绿假单胞菌药敏表格。如果实验室按照Z新的CLSI规范报告结果,建议在此类中介加上如下备注:“此药物可在尿液中浓缩,并在其他解剖部位(如:上皮衬液)也存在浓缩可能性”。
05 头孢地尔和达托霉素的相关更新
1. 头孢地尔
头孢地尔是新上市的铁载体-头孢菌素类KJ药物,对CRO的ZL提供了更多的方案,是被大家寄予厚望的新一代头孢菌素。因此去年和今年均对此KJ药物的药敏方法进行了大量的更新,在2020年的主要更新为增加了头孢地尔纸片法的折点,并增加了1个专门的附录用来详细说明头孢地尔肉汤制备流程和肉汤微量稀释MIC终点判读。
目前头孢地尔纸片法新增的折点如下:
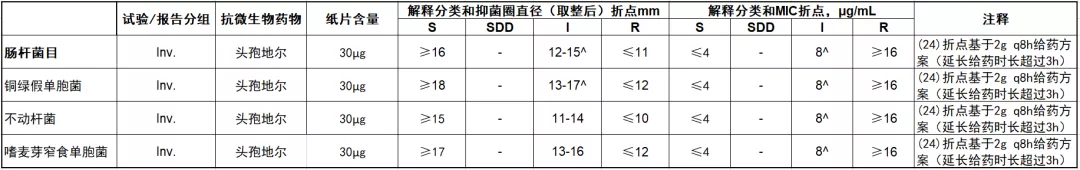
目前头孢地尔肉汤微量稀释法需要特殊的培养基去铁离子阳离子调节肉汤(IDCAMHB),制备较为繁琐,但纸片法却不需要使用。
2. 达托霉素
今年对于达托霉素的更新主要集中在屎肠球菌方面,重新更新了折点,添加了相关备注。
更新后的达托霉素折点如下:
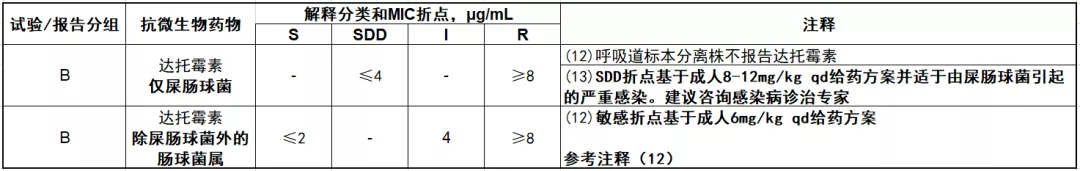
即对于屎肠球菌,达托霉素目前只有SDD和R的折点,没有敏感折点。而对于SDD建议后面直接加上注释(13)的相关内容“SDD折点基于成人8-12mg/kg qd给YF案并适于由屎肠球菌引起的严重感染。建议咨询感染病诊治专家。”
06 KB法方面的更新
在所有的折点表格前,大家可以发现这样一条加黑更新:量取KB法直径时,可以参考M02纸片法阅读指南,这其实指的18年CLSI在M02文件更新时,同步发布的M02 QG文件。此文件图文并茂的展示了如何规范的测量YJ圈直径。建议目前仍使用KB法作为主要药敏检测方法的实验室做到人手一份。
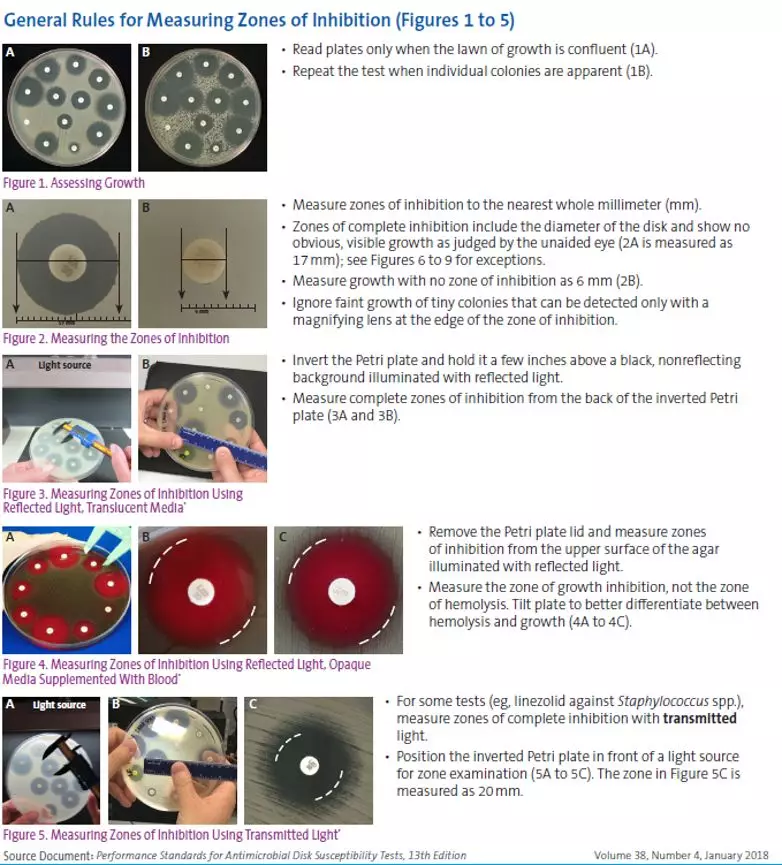

还有一个比较重要的更新,就是在进行肺炎链球菌KB法药敏时候,增加了MH-F琼脂(MH苛养琼脂)。此琼脂是EUCAST推荐的苛养菌用药敏琼脂,目前使用此琼脂量取的链球菌YJ圈直径和5%绵羊血MH琼脂具备等效关系。
笔者注:下表为笔者做的苛养菌药敏培养基EUCAST和CLSI两种规范的比较,从中可以看出EUCAST相对比较简单,统一使用MH-F琼脂和MH-F肉汤,而CLSI提供了多种肉汤和琼脂平板,因此如果以后此两种规范在苛养菌的药敏培养基上达成了一致,苛养菌的药敏试验就可以方便许多。(去年做链球菌和嗜血杆菌药敏试验配培养基到头晕眼花的笔者有感而发)

07 质控方面的更新
质控方面的更新是我们比较容易忽视的,因为确实一般不会影响到我们的药敏试验和药敏结果的解释分析,但是通过质控增加的新药我们可以了解到在美国上市(或即将上市)的Z新KJ药物以及对于新耐药机制检测至关重要的质控菌株。
1. 新增药物
今年CLSI新增加的药物有8个,简单可以分为3大类,一个是头孢吡肟+新一代的β-内酰胺酶合剂;另一个是舒巴坦相关的β-内酰胺酶合剂。Enmetazobactam和Taniborbactam是两个新一代的β-内酰胺酶YZ剂,这些酶YZ剂可能可以有效的YZB类金属酶,因此可以有效的ZLCRE;目前尚处于早期临床阶段。而舒巴坦-durlobactam,是专门用于ZL泛耐药鲍曼不动杆菌新型KJ药物,是一个专门针对泛耐药鲍曼不动杆菌的KJ药物。其他还有3个新药 Exebacase为抗葡萄球菌的溶解酶,主要针对MRS;Ozenoxacin是新的喹诺酮类药物;而Zoliflodacin是一种抗淋病奈瑟菌的新药。
新增的5个β-内酰胺酶合剂KJ药物,及其质控菌株列表
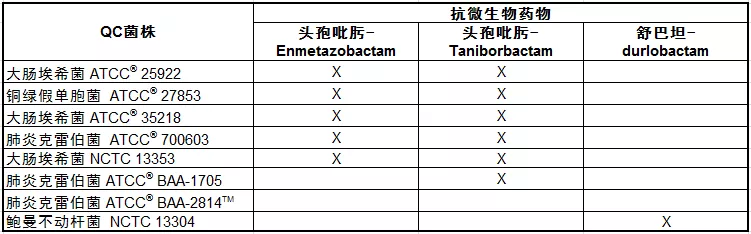
其他3个新增药物
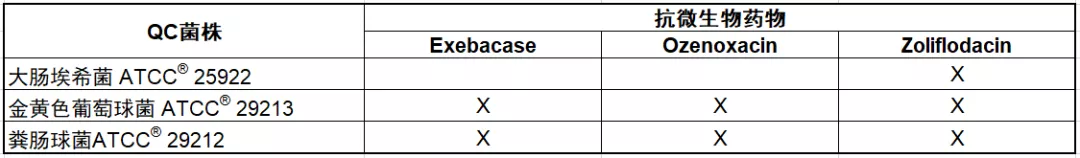
2. 新增质控菌株
今年新增的质控菌株主要与多粘菌素类KJ药物的药敏质控相关,是一株携带有MCR-1耐药基因的大肠埃希菌,编号为AR Bank #0349。
笔者注:这么奇怪的编号,也不是ATCC和NCTC的标准菌株,国内目前有无购买渠道呢?
08 其他更新
其他比较小的更新还包括去年从各项表格中删除的诺氟沙星又加回来了,给了红霉素诱导克林霉素耐药一个专用缩写ICR,嗜麦芽窄食单胞菌中将左氧沙星和米诺环素从B组药物上移到A组药物中。以及其他一些较小更新。

参考资料
[1] Tsuji BT, Pogue JM, Zavaxcki AP, et al. International consensus guidelines for the optimal use of the polymyxins: endorsed by the American College of Clinical Pharmacy (ACCP), European Society of Clinical Microbiology and Infectious Diseases (ESCMID), Infectious Diseases Society of America (IDSA), International Society for Anti-Infective Pharmacology (ISAP), Society of Critical Care Medicine (SCCM), and Society of Infectious Diseases Pharmacists (SIDP). Pharmacotherapy. 2019;39(1):10-39.
[2] Adeolu M, Alnajar S, Naushad S, Gupta RS. Genome-based phylogeny and taxonomy of the ‘Enterobacteriales’: proposal for Enterobacterales ord. nov. divided into the families Enterobacteriaceae, Erwiniaceae fam. nov., Pectobacteriaceae fam. nov., Yersiniaceae fam. nov., Hafniaceae fam. nov., Morganellaceae fam. nov., and Budviciaceae fam. nov. Int J Syst Evol Microbiol. 2016;66(12):5575-5599.

 评论
评论