发布:
培安(中国)有限公司时间:
2022-08-15行业:
生物产业 综合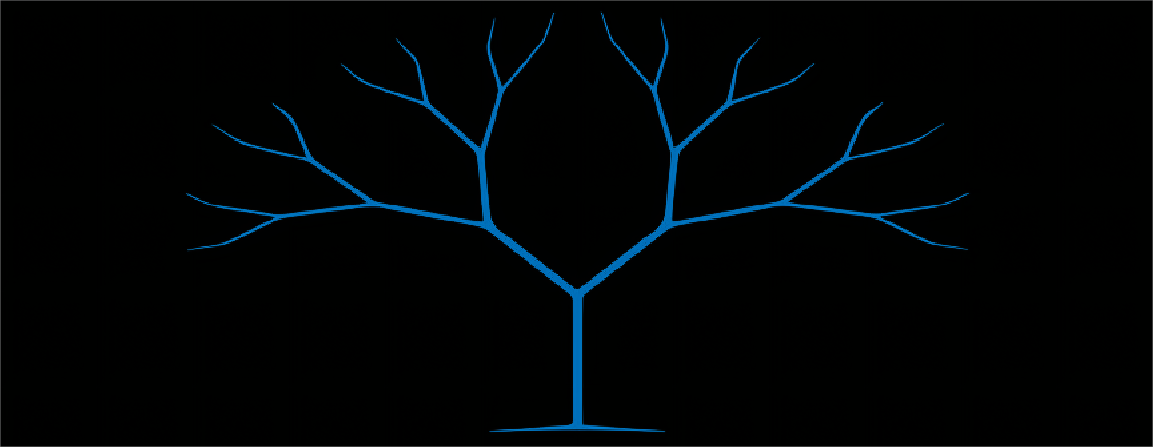
摘要
微波增强的多肽固相合成(SPPS)可以合成具有对称赖氨酸分支的多抗原肽(MAPs)或多肽树枝状大分子,合成时间大幅降低,纯度提高。四分支酰基载体蛋白(ACP)肽的合成在2小时内完成,纯度为70%。四分支M10肽1(巴西副球孢子菌糖蛋白T细胞表位)的合成在4小时内完成,纯度为50%。在2小时内合成纯度为80%的一个八聚体,第三代赖氨酸-亮氨酸抗jun肽树枝状大分子(G3KL)2。
引言
对称分支肽(图1)代表一类具有非常理想的理化和生物学特性的肽。在一些情况下,由于与蛋白质靶标的多价结合或具有更高的蛋白酶抗性,包含分支核心的肽,如多抗原肽(MAPs)或肽树状聚合物有更高的生物活性3。因此分支肽已被用于各种治疗应用,包括开发抗微生物和抗病du药物4,5、肿瘤靶向剂6,7和药物输送载体8。
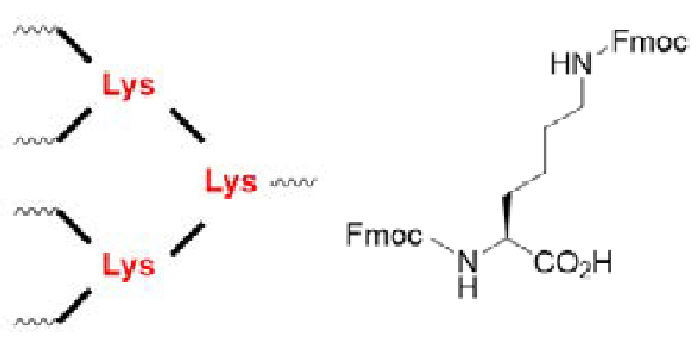
图1:左:对称分支的赖氨酸核心;
右:Fmoc-Lys(Fmoc)-OH
对称分支肽的合成可通过在SPPS中使用Fmoc-Lys(Fmoc)-OH来生成支链位置。合成通常比较困难,因为在分支支架上肽链固有的紧密接近性,会导致空间冲突和肽偶联不良。将微波能量应用于分支肽的合成克服了这些空间挑战,允许更有效的偶联和快速合成较少缺失的困难分支肽产物 (CarboMAXTM)。9
材料和方法
试剂
以下含有特定侧链保护基团的Fmoc氨基酸购自CEM公司(Matthews, NC):Arg(Pbf)、Asn (Trt)、Asp (OtBu)、Gln(Trt)、His (Boc)、Lys (Boc)、Tyr (tBu) 和Thr (tBu)。Rink Amide ProTide LL 树脂也得自CEM 公司。Fmoc-6-Ahx-OH 购自AnaSpec (Fremont, CA)。Fmoc-Lys(Fmoc)OH 获自 CreoSalus (Louisville, KY)。N,N'二异丙基碳二亚胺(DIC)、哌啶、三氟乙酸(TFA)、3,6-二氧六环-1,8-辛二硫醇(DODT) 和三异丙基硅烷(TIS) 购自Sigma-Aldrich (St. Louis, MO)。二氯甲烷(DCM)、N,N-二甲基甲酰胺(DMF)、无水乙mi(Et2O)、乙酸、HPLC 级水和乙腈购自VWR (West Chester, PA)。LC-MS 级水(H2O) 和LC-MS 级 乙 腈 (MeCN) 购 自 Fisher Scientific (Waltham, MA)。
多肽合成:四分支ACP, (VQAAIDYING)4-(K)2-K-Ahx-KK-NH2
使用CEM Liberty BlueTM 自动微波肽合成仪在Rink Amide ProTide LL 树脂(离子交换容量:0.19 meq/g)上以0.1 mmol 规模(树脂规模:0.025 mmol)制备肽(下图)。用哌啶和Oxyma Pure 在DMF 中进行脱保护。在 DMF (CarboMAX) 9中,五倍过量的Fmoc-AA 与DIC 和Oxyma Pure 进行偶联反应。Fmoc-Lys(Fmoc)-OH 用于分支位置的K。使用带有 TFA/H2O/ TIS/DODT 的CEM RazorTM 高通量肽切割系统进行切割。切割后,用无水乙mi沉淀肽并冻干过夜。
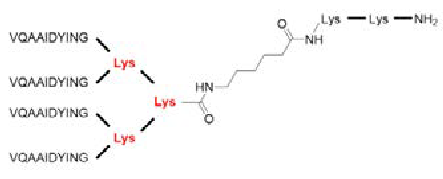
Tetra-branched ACP
多肽合成: 四分支M10, (LIAIHTLAIRYAN)4-(K)2-K-Ahx-KK- NH2
使 用 CEM Liberty BlueTM 自 动 微 波 肽 合 成 仪 在 Rink Amide ProTide LL 树 脂(离 子 交 换 容 量 :0.19 meq/g)上 以 0.1 mmol 规模(树脂规模:0.025 mmol)制备肽(下图)。用哌啶和 Oxyma Pure 在DMF 中进行脱保护。在 DMF 中 5 倍过量的Fmoc-AA 与DIC 和Oxyma Pure 进行偶联反应( CarboMAX)9。Fmoc-Lys(Fmoc)-OH 用于分支位置的K。使用带有 TFA/H2O/TIS/DODT 的CEM RazorTM 高通量肽切割系统进行切割。裂解后,用无水乙mi沉淀肽并过夜冻干。
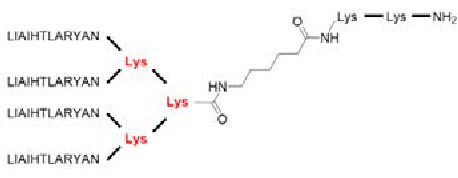
Tetra-branched M10
多肽合成:G3KL 八聚体, (KL)8-(KKL)4-(KKL)2-KKL-Ah-KK-NH2
使 用 CEM Liberty Blue 自 动 微 波 肽 合 成 仪 在 Rink Amide ProTide LL 树脂(离子交换容量:0.19 meq/g)上以0.25 mmol 规模(树脂规模:0.025 mmol)制备肽(下图)。用哌啶和Oxyma Pure 在DMF 中进行脱保护。在 DMF 中5倍过量的 Fmoc-AA 与DIC 和Oxyma Pure 进行偶联反应(CarboMAX)9。Fmoc-Lys(Fmoc)-OH 用于分支位置的K。使用具有TFA/H2O/TIS/DODT 的 CEM Razor 高通量肽切割系统进行切割。裂解后,用无水乙mi沉淀肽并冻干过夜。
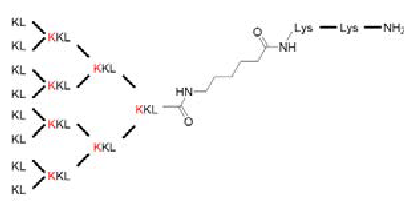
G3KL Octamer
多肽分析
在配备有 PDA 检测器的 Waters Acquity UPLC 系统上分析肽,该 检 测 器 配 备 Acquity UPLC BEH C8 柱(1.7mm 和2.1×100mm)。UPLC 系统连接到Waters 3100 Single Quad MS 用于结构测定。在 Waters MassLynx 软件上进行峰值分析。在 (i)H2O 和 (ii)MeCN 中以0.05% TFA的梯度洗脱进行分离。
结果
Liberty Blue 自动微波肽合成仪上的使用微波增强 SPPS 合成四分支的ACP多肽,产生了 70% 纯度的目标肽(图2)。
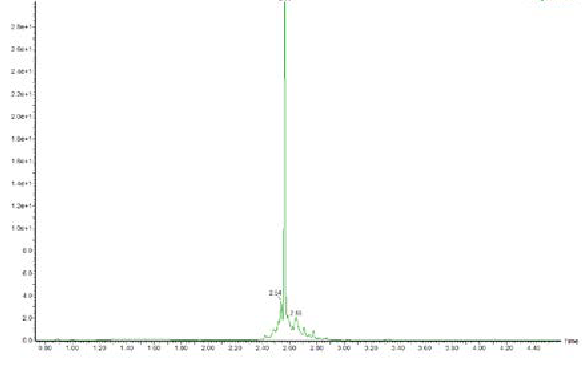
图2:四分支ACP的UPLC色谱图
Liberty Blue 自动微波肽合成仪上使用微波增强 SPPS 合成在Liberty Blue 自动微波肽合成仪上使用微波增强 SPPS 合成 G3KL 八聚体产生了 80% 纯度的目标肽(图4)。
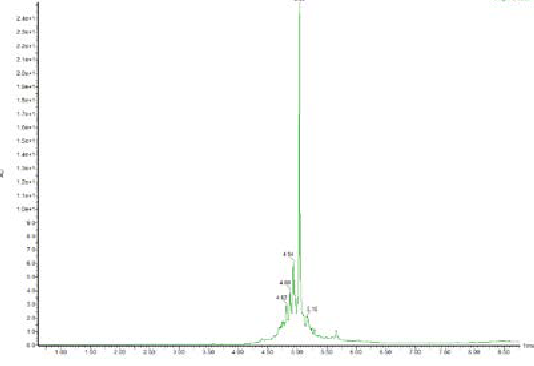
图3:四分支M10的UPLC色谱图
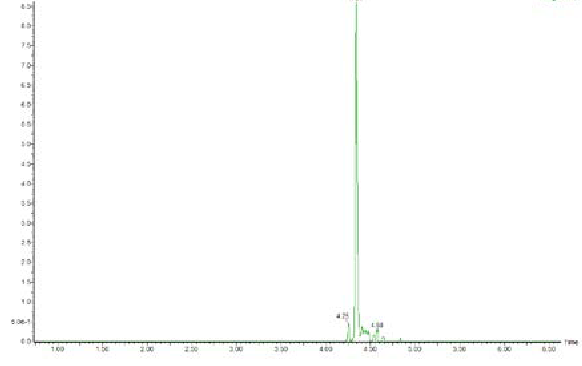
图4 :G3KL八聚体的UPLC色谱图
结论
与传统的 SPPS 方法相比,使用微波增强的 SPPS 可以更快地制备对称分支肽,并且纯度更高。使用微波增强 SPPS,在2小时内合成了纯度为 70% 的四分支 ACP。四支化 M10 肽的常规室温合成需要超过42小时的手工劳动,目标肽的分离产率为 4%。
另一方面,微波增强的 SPPS 可在4小时内提供纯度为50%。G3KL 八聚体的常规合成需要超过35小时的手工劳动时间,并以 8% 的分离产率产生目标肽。2 将微波能量应用于 G3KL 八聚体的合成可在2小时内以 80% 的纯度提供目标肽 。
参考文献
[1] Taborda, C. P.; Nakaie, C. R.; Cilli, E. M.; Rodrigues,E.G.;Silva, L. S.; Franco, M. F.; Travassos, L. R. Scand. J. Immunol. 2004, 59 (1), 58–65.
[2] Stach, M.; Siriwardena, T. N.; Köhler, T.; van Delden, C.; Darbre, T.; Reymond, J.-L. Angew. Chemie Int. Ed. 2014, 53 (47), 12827–12831.
[3] Falciani, C.; Lozzi, L.; Pini, A.; Corti, F.; Fabbrini, M.; Bernini, A.; Lelli, B.; Niccolai, N.; Bracci, L. Chem. Biol. Drug Des. 2007, 69 (3), 216–221.
[4] Liu, S. P.; Zhou, L.; Lakshminarayanan, R.; Beuerman, R. W. Int. J. Pept. Res. Ther. 2010, 16 (3), 199–213.
[5] Wynn, J. E.; Santos, W. L. Org. Biomol. Chem. 2015, 13 (21), 5848–5858.
[6] Falciani, C.; Pini, A.; Bracci, L. Expert Opin. Biol. Ther. 2009, 9 (2), 171–178.
[7] Minervini, A.; Siena, G.; Falciani, C.; Carini, M.; Bracci, L. Expert Rev. Anticancer Ther. 2012, 12 (6), 699–701.
[8] Brunetti, J.; Pillozzi, S.; Falciani, C.; Depau, L.; Tenori, E.; Scali, S.; Lozzi, L.; Pini, A.; Arcangeli, A.; Menichetti, S.; Bracci, L. Sci. Rep. 2015, 5, 17736.