间充质干细胞质量控制
2019-09-27576间充质干细胞药物制剂的质量控制
干细胞是指具有自我更新和分化能力的细胞类型。间充质干细胞(Mesenchymal Stem Cell)是来源于中胚层的一种成体干细胞,主要存在于牙髓、脂肪、脐带、羊膜、经血等组织中。
间充质干细胞具有免疫原性低,增殖能力强、免疫调节、趋化功能以及分泌等功能,同时在特定的体内环境中,以及人为控制的体外培养环境中分化为脂肪细胞、软骨细胞、心肌细胞、神经细胞、肝细胞、成骨细胞、基质细胞等多种细胞类型。由于间充质干细胞具有以上特性功能,所以在免疫性疾病、退行性疾病以及肝肺纤维化以及代谢类疾病中具有非常广阔的临床应用前景。
间充质干细胞制备是通过采集供者牙髓、经血、、脂肪、脐带、胎盘或羊膜等组织,经过体外的分离、扩增、鉴定等生产质控流程后,回输到患者人体的ZL方法。相比于其他药物类型,间充质干细胞药物具有流程长,操作复杂,风险点多,过程控制难等特点。因此严格的生产及质量控制对干细胞药物非常重要。
间充质干细胞药物与常规生物制品不同,首先细胞来源于人体组织,生产制备过程包括细胞分离、细胞扩增、细胞传代、细胞消化、细胞冻存、细胞运输等多种复杂程序。而且Z终药物制剂是有生命的活细胞,中间使用的试剂耗材种类繁多,因此确定规范流程以及原料使用非常重要。
根据已有报道,间充质干细胞质量控制大致分为以下几点:
1、 来源控制
2、 流式鉴定
3、 核型分析
4、 细胞活率检测
5、 细胞分化能力检测
6、 端粒酶分析
7、 残留检测
8、 冻存后细胞复苏能力检测
9、 放行检测规范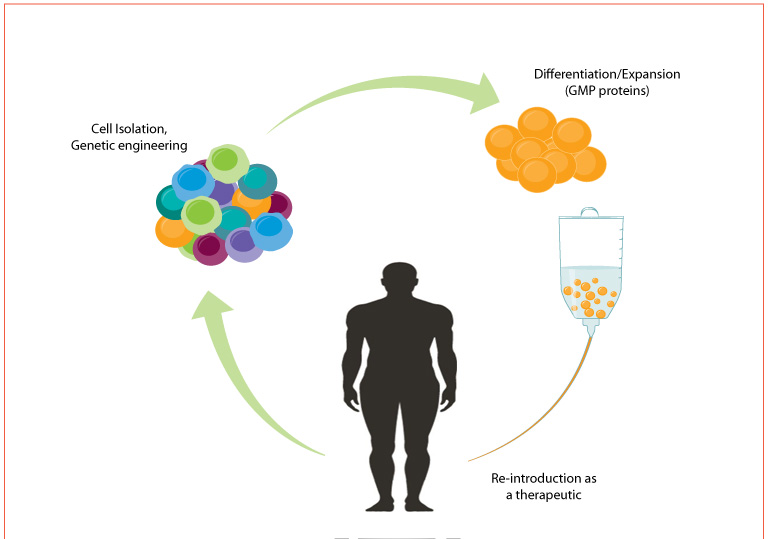
间充质干细胞因其来源多样,生产过程复杂,中间会引入生长因子,蛋白酶,等外来成分,同时还有潜在细菌,支原体以及潜在的病毒污染。同时药物制剂为活细胞,需要短时间内回输,或冻存后回输。从产品的制备到使用的整个链条中,如何保证细胞的活性、生物学功能稳定性、遗传特征稳定性、质量可控性,直接关系到临床应用的安全和有效。因此指定严格的细胞生产及质控规范,有效过程控制以及试剂原料的严格筛选对IND临床申报必不可少。后续我们将针对生产及质量控制进行深入分析,以希望对干细胞临床申报提供合适的建议及合规的产品。
参考文献:
1、 耿洁,张磊,韩之波,王有为,王斌,韩忠朝 临床用间充质干细胞的质量控制研究 ZG医药生物技 .2013年6月第8卷第3期
2、 陈文庆,罗海春,邹武科 细胞培养基的质量控制与GMP管理ZG医药生物技术2007年2月第2卷第1期
3、 胡泽斌,王立生,崔春萍,陈津,吴祖泽,谢俊祥,吴朝晖 干细胞临床应用安全性评估报告 ZG医药生物技术 2013 年10 月第8 卷第5 期

