实验方案
中成药成分含量测定
针对中成药的国家组织药品集中带量采购最近落地。这是自2018年国家药品集采改革以来,继化学药、生物药、医用耗材的国家集采之后,首次对中成药开展国家集采。
中成药国家集采常态化,将促进中成药提质降价,既可以挤掉中成药虚高的价格水分,也可以降低医保费用支出,同时推动中药行业优胜劣汰。
中成药作为我国特有的中药制剂,品种众多、剂型多样、临床应用范围广泛。随着中药现代化进程的不断推进,中成药产业发展迅速,作为临床直接使用的药品,其质量直接关系到民众用药安全与疗 效。
含量差别大、掺伪、染色、批间质量差异大等问题,给中成药质量带来风险。对其进行质量控制与评价意义重大。
中成药的质量评价,可以借助严谨的实验进行,我们选取一种中成药,通过测定其中的有效成分含量,为中成药质量评价提供依据。
此次实验,使用悟空K2025高效液相色谱仪测定归芷白癫康颗粒中芍药苷的含量。
一、实验方案
实验原理:
归芷白癫康颗粒样品中的芍药苷经HPLC反相色谱柱分离,用紫外检测器检测,外标法定量。
《山东省医疗机构制剂规范(第 一版第四册,附件1)》中含量测定里面规定归芷白癫康颗粒每袋含赤芍以芍药苷计,不得少于2.0 mg。
色谱条件:
悟空K2025高效液相色谱仪:K2025 P2二元高压输液泵、K2025 AS自动进样器、K2025 CO柱温箱、K2025 UVD紫外-可见光检测器、Wookinglab色谱工作站;

色谱柱:C18 色谱柱,4.6×250 mm,5 μm或者相当的色谱柱;
流动相:甲醇:水=22:78;
柱温:25℃;
进样量:10 μL;
流速:1.0 mL/min;
波长:230 nm。
二、实验结果
1、重复性测试
按照色谱条件进行采集,芍药苷标准溶液(浓度为43.180 µg/mL)的色谱图如图1所示,积分结果如表1所示。
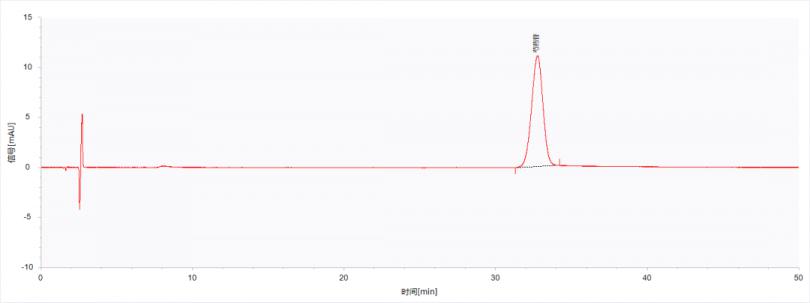
图1芍药苷标准溶液的色谱图
表1 芍药苷标准溶液色谱图积分结果

由表1可知,芍药苷的理论塔板数为9061,完全满足附件1里规定的理论塔板数按芍药苷峰计算应不低于2000的要求。
将芍药苷标准溶液连续进样7针,叠加的色谱图如图2所示,结果见表2。
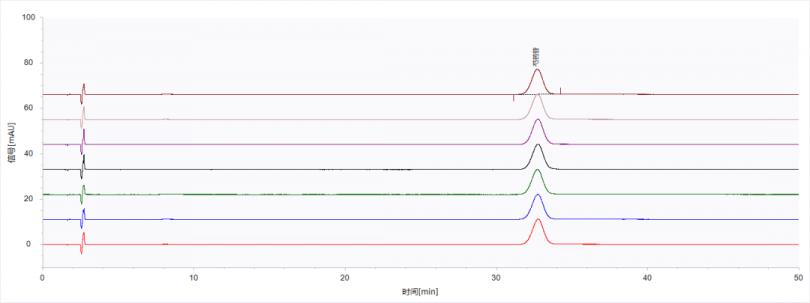
图2芍药苷标准溶液连续进样7针叠加的色谱图
表2芍药苷标准溶液连续进样7针重复性数据统计
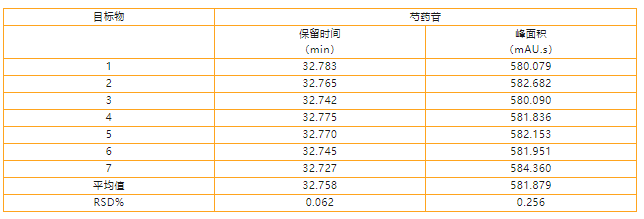
由表2可知,芍药苷标准溶液连续进样7针,保留时间的RSD为0.062%,峰面积的RSD为0.256%。
2、含量测定
校准曲线
将配制好的芍药苷标准工作液在HPLC上进行测定,叠加色谱图见图3。芍药苷在测定浓度范围内,曲线的相关系数R2达到0.9996,线性关系良好。
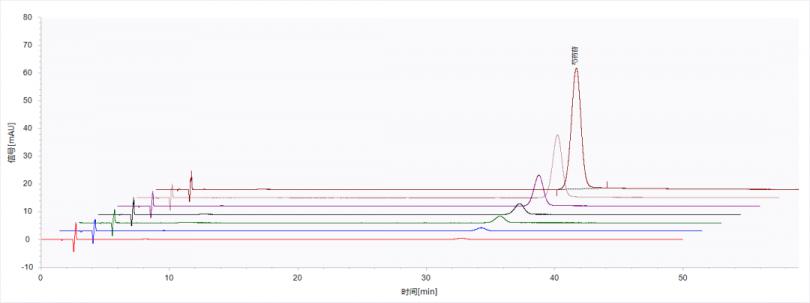
图3 芍药苷标准溶液浓度系列曲线叠加色谱图
样品含量测定
取归芷白癫康颗粒样品(批号分别是20220119和20210929)按照流程进行处理。样品的色谱图如图4及图5所示,样品中芍药苷的含量见表3。
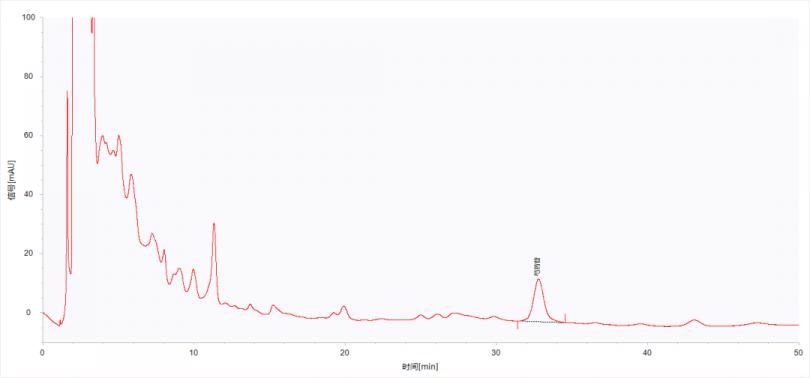
图4 样品(批号为20210929)的色谱图
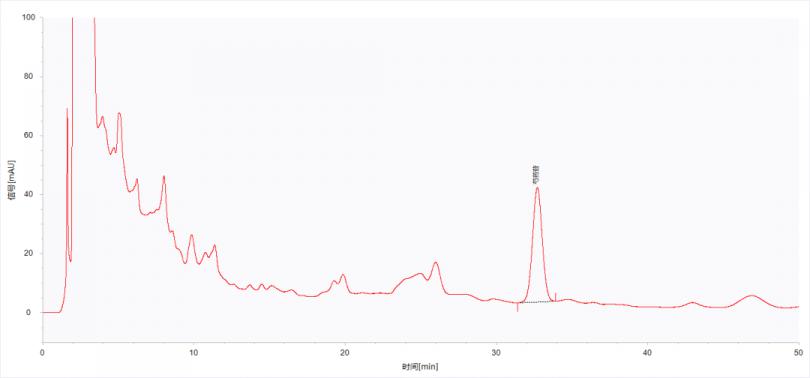
图5 样品(批号为20220119)的色谱图
表3 样品中芍药苷的含量
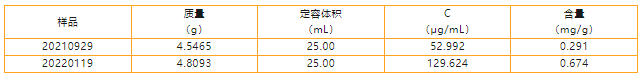
样品(批号为20210929和20220119)的规格为12 g/包,经计算,样品(批号为20210929)每袋中含芍药苷3.492 mg,样品(批号为20220119)每袋中含芍药苷8.088 mg。
三、结论
通过对芍药苷的理论塔板数、重复性、灵敏度、线性的测试以及归芷白癫康颗粒样品的测试,实验结果表明:
用K2025测定芍药苷的理论塔板数为9061,完全满足《山东省医疗机构制剂规范(第 一版第四册,见附件1)》里规定的理论塔板数按芍药苷峰计算应不低于2000的要求;
在重复性测试中,将芍药苷标准溶液连续进样7针,保留时间的RSD为0.062%,峰面积的RSD为0.256%,定性定量均有良好的重复性;在测定浓度范围内,芍药苷具有良好的线性关系,确定系数R2为0.9996;芍药苷的仪器检出限为0.426 µg/mL,仪器定量限为1.420 µg/mL;样品(20210929)每袋中含芍药苷3.492 mg,样品(20220119)每袋中含芍药苷8.088 mg。
因此,Wooking K2025高效液相色谱仪可以满足《山东省医疗机构制剂规范(第 一版第四册,附件1)》中归芷白癫康颗粒中芍药苷含量测定的要求。
中成药质量问题涉及中药材种植、饮片炮制和流通、药品生产和贮藏等诸多环节,但是核心问题仍然是中成药质量控制的问题。
围绕中药质量安全、有效和稳定可控开展中药质量控制研究,完善和提高质量标准,有助于促进中药现代化进程。
消费者也可全面认识和考虑诸多因素对中成药疗 效的影响,更加安全有效、经济、适当使用中成药。
 悟空液相产品即将发布
悟空液相产品即将发布

 评论
评论