
今天的蛋白组学研究中,研究人员们在转化研究,生物标志物发现,甚至单细胞分析等过程中,不止是追求简单的鉴定,更多的需要获取准确可靠的定量信息,用以理解生物学问题。 他们需要使用精确的定量检测方法来表征生物系统之间的差异,对大量样本进行高置信度、高通量的表征,验证生物学假说。
在刚结束的USHUPO中,赛默飞正式推出了全新的Velocity LFQ DIA 工作流程。 该平台基于Thermo Scientific Orbitrap 超高分辨质谱仪、Thermo Scientific Vanquish NEO UHPLC 系统以及高效的 Thermo Scientific µPAC UHPLC 色谱柱技术,具有优异的定量性能,蛋白组深度覆盖,并可轻松实现高通量分析,匹配今天研究人员们对定量蛋白组学研究的需求。 下面就由小编给大家介绍该平台的工作流程,并展示其在定量表征、蛋白组覆盖度和方法通量中的性能。
Workflow
Velocity LFQ DIA 工作流程
Velocity LFQ DIA 工作流程组成如图1 所示,包括Vanquish Neo UHPLC 系统和µPAC Neo UHPLC 色谱柱用于色谱分离,Easy-Spray 纳升离子源和 Orbitrap Exploris 240/480 用于质谱数据采集,Spectronaut软件用于数据分析。

图1. Velocity LFQ DIA 工作流程示意图
(点击查看大图)
色谱分离:
大队列研究中需要有稳健的色谱设置(分离技术、色谱柱等),确保系统长期稳定运行。 Vanquish Neo UHPLC 系统可实现高重现性,并可进行多种类型的 LC-MS 实验。 新的色谱分离技术同样也可提高系统稳健性,例如基于微阵列的 µPAC Neo 色谱柱,可提高分析灵敏度和保留时间稳定性 [1] 。
质谱分析:
除了稳健性和重复性之外,可靠的鉴定和定量在蛋白组学研究中十分重要。 Orbitrap 技术可提供高质量精度以及高分辨率,是复杂 DIA 扫描中可靠鉴定,以及准确、精确检测并分辨离子类型的关键因素。
数据分析:
DIA谱图中为混合母离子碎裂后所得的混合子离子谱图,通常需要使用谱图库方法进行解析。 但是,随着数据分析软件(例如,使用机器学习方法模拟预测获得高质量的谱图库)的发展,无需谱图库的方法成为了节约时间和成本的一种选择。
Key Words
Velocity LFQ DIA 工作流程三个关键词:
定量、覆盖度、通量
为了深入展示 Velocity LFQ DIA的性能,我们建立一个稳健、高重现性的工作流程,可实现复杂样品中蛋白的准确鉴定和定量。 其中使用了两个不同的混合样品,包括两种蛋白组和三种蛋白组混合样品(图2),质谱数据采集使用OE240质谱仪。
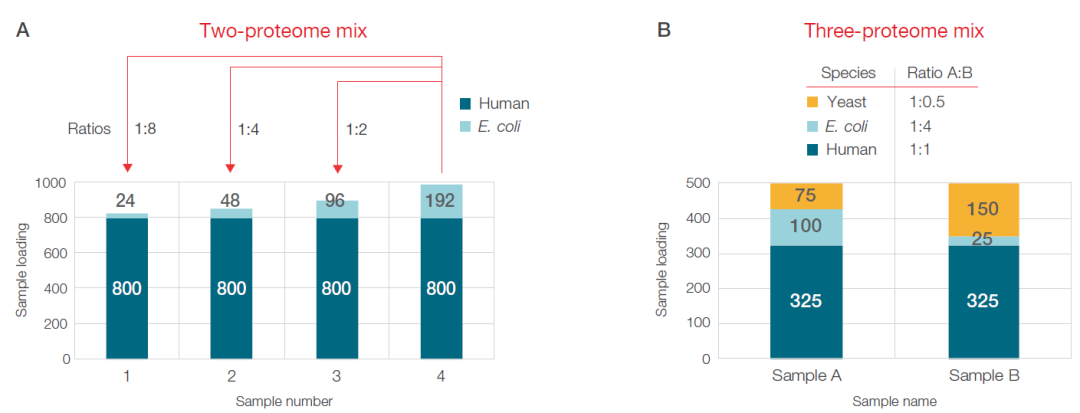
图2. Velocity LFQ DIA 工作流程性能展示所使用的的实验设计。 A,两种蛋白组混合样本,包括高含量的人类肽段背景(800 ng Hela 酶解肽段),低到中含量的 Ecoli肽段,比值为1:2:4:8; B,三种蛋白组混合样本,中等含量的人类肽段背景(325 ng Hela 酶解肽段),以及酵母和Ecoli肽段,比值分别为1:0.5和1:4。 这些混合样本分别模拟生物样本中的上调和下调蛋白表达情况。 (点击查看大图)
01
出色的定量性能
分别对上述两种样本进行30min的LC-MS采样,数据采用Spectronaut16,directDIA的方式进行数据分析,肽段和蛋白的FDR均小于1%。
Ecoli和hela的混合样本中,ecoli蛋白在4个样本中的3个不同比值均十分接近理论比值,且所有数据点在中位数附近分布很窄,展示了Velocity LFQ DIA工作流程的高定量准确性和精密度(图3A)。 此外,技术重复间肽段的 CV 值均小于 7%(图3B),说明该工作流程具有高定量精密度。
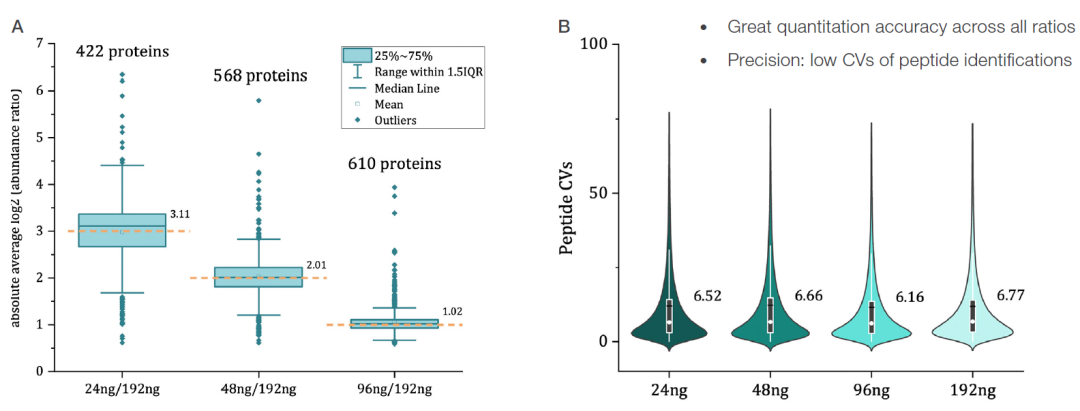
图3. 工作流程的定量准确性和精密度展示,使用两个蛋白组混合样本。 A,Ecoli蛋白三个不同比值下的实际比值,以箱型图展示,橙色虚线为理论比值; B,4个不同比例下肽段丰度CV的小提琴图。 (点击查看大图)
同时,使用Velocity LFQ DIA工作流程可获得约5个数量级的人类蛋白动态范围(图4A),有助于低丰度蛋白的发现。 在高含量的hela肽段背景下,使用该工作流程可发现很多细菌体内的重要蛋白,包括与转录翻译相关,以及人类干扰素诱导相关的ecoli蛋白。 另外,选取了Ecoli中十个丰度最低的蛋白,发现它们在不同样品间的实际比值依然十分接近理论比值(图4B),说明该工作流程即使在低丰度蛋白情况下仍可获得高定量准确性。
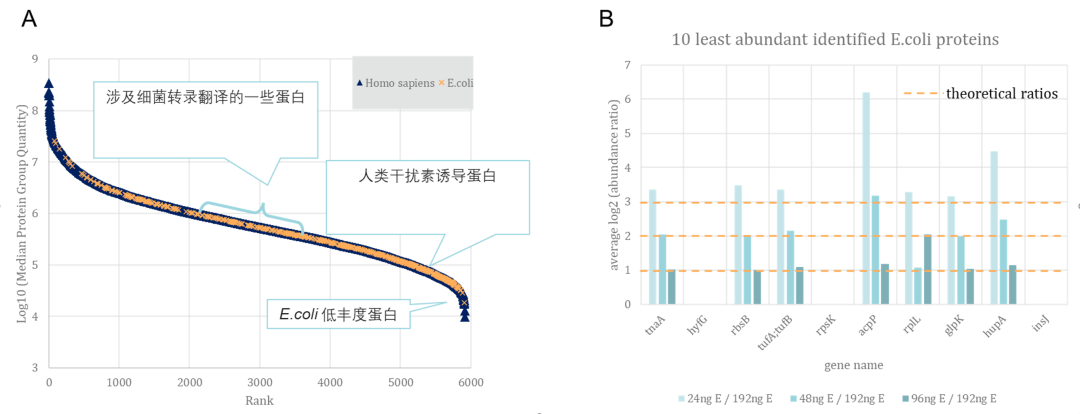
图4. A,两个蛋白组混合样本的蛋白丰度分布; B,Ecoli中十个丰度最低蛋白的实际比值与理论比值偏差 (点击查看大图)
在三个蛋白组混合样本中,Velocity LFQ DIA工作流程同样展示了出色的定量性能。 实际比值与理论比值之前偏差<2%。 可定量约3000个人类蛋白,接近500个Ecoli蛋白(图5 A)。 样本A与B的肽段丰度展现了与比值相一致的线性斜率,以及与物种相关的整体丰度范围(图5B)。
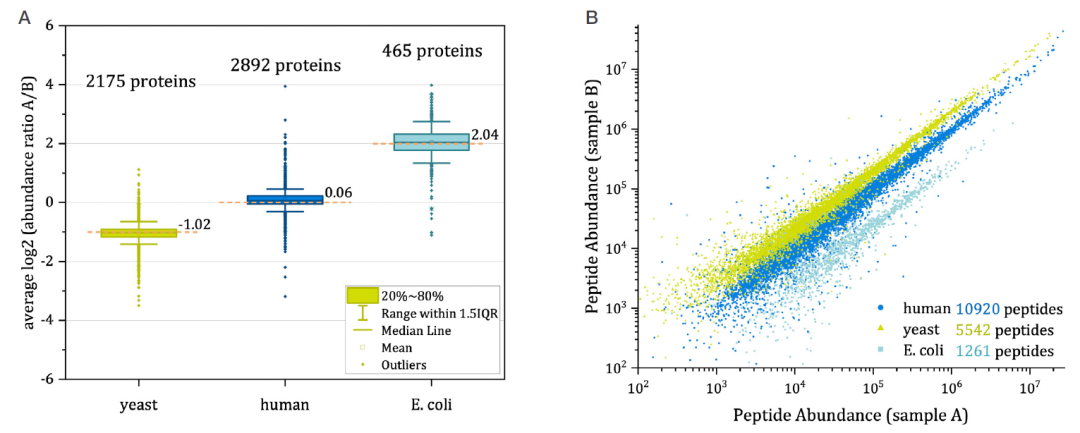
图5. 工作流程的定量性能展示,使用三个蛋白组混合样本。 A,三个蛋白组不同比值下的实际比值,以箱型图展示,橙色虚线为理论比值; B,样本A与B的肽段丰度相关性。 (点击查看大图)
02
深度蛋白组覆盖
使用Spectronaut16的directDIA方法分析两个蛋白组样品,在不损失定量性能的同时,可获得深度蛋白组覆盖。 然后使用第三方软件DIA-NN [2] 分析相同的数据集,可获得与sp16类似的结果。 当使用Spectronaut17软件时,改善的directDIA+方法可提高30%的母离子鉴定,及10%的蛋白鉴定(图6),30min梯度内,不使用谱图库可获得接近7000个蛋白鉴定。 这表明Velocity LFQ DIA工作流程不仅可获得出色的定量性能,也可实现深度蛋白组覆盖,此外也说明了不使用谱图库可作为一种有效的DIA数据分析方法。 如果想进一步提高蛋白组覆盖深度,也可通过建立合适谱图库的方法实现。
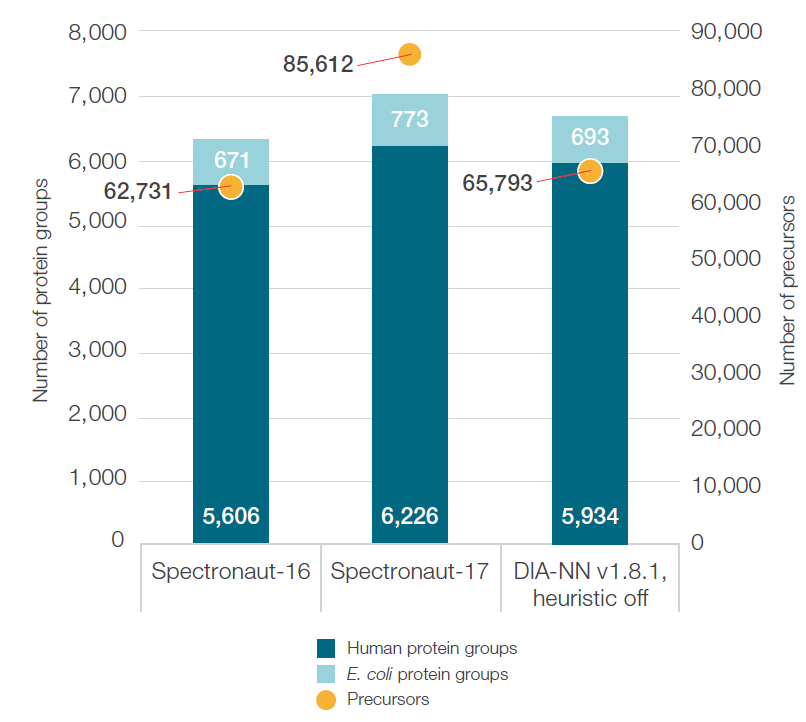
图6. 使用library free方法分析两个蛋白组样品可实现深度蛋白组覆盖。 柱状图比较了三个不同的软件(或版本)所得的蛋白和母离子数目,FDR<1%。 (点击查看大图)
03
高通量流程
在上述所展示的Velocity LFQ DIA工作流程中,有效梯度为30min,实际时长为每针39min,可提供每天分析 36个样品的通量。 另外,在一些大队列研究中,研究人员需要更高的分析通量。 在Velocity LFQ DIA工作流程中使用了Vanquish Neo液相,其使用灵活,且经过优化样品吸取、上样、色谱柱清洗和平衡等流程,可有效提高质谱利用率 [3] ,可方便研究人员根据项目需求,进一步提高样品通量。
04
工作流程稳健性
为了验证Velocity LFQ DIA工作流程的稳健性,从一个持续两个月时间(使用同一根色谱柱)的项目中选取其中的一部分数据作为展示。 采用 200 ng Hela肽段,DDA实验作为系统性能的 QC,在两个月内间歇运行,梯度为67min,结果如图7所示。 由结果可知,肽段和蛋白的鉴定数字在整个500小时的项目中(总上样量约为130 µg)保持一致(鉴定数字变化在5%以内)。 这说明了色谱柱,色谱分离以及质谱的稳健性,这对大队列研究十分重要,是获得良好数据的基础。
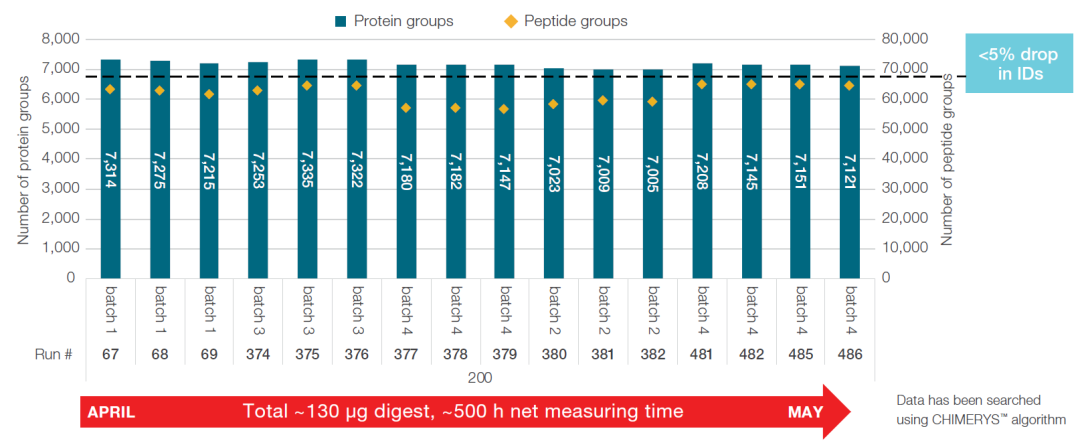
图7. 两个月的使用时间内,肽段和蛋白鉴定的重现性。 在整个实验周期中,间歇运行DDA QC实验,数据分析使用CHIMERYS算法。 (点击查看大图)
小结
Velocity LFQ DIA工作流程结合了 Vanquish Neo 系统,µPAC Neo色谱柱以及 Orbitrap 超高分辨质谱仪,是高通量非标蛋白组DIA鉴定和定量的一种理想工作流程。
采用30min梯度的OE240方法展示了该工作流程的主要性能特点: 出色的定量深性能、蛋白组深度覆盖和分析高通量。
Velocity LFQ DIA工作流程适用于需要高通量、稳健性、高准确性精密度定量性能和深度蛋白组覆盖的定量蛋白组学研究。

 评论
评论