神经母细胞瘤(Neuroblastoma)是儿童、婴幼儿较为常见的一种颅外肿瘤。其典型的特点是后期恶性化程度较高,预后较差。为保证药物具有针对性,提高治愈率,目前推荐的一个策略是在组织模型中确定病人对该药物的特异性反应。因此,构造一个具有肿瘤微环境的特异性组织模型就显得尤为重要。
目前,构建肿瘤微环境的一个主要难点在于如何触发其形成血管并发生肿瘤血管化(Tumor-vascularization)。已有的尝试主要为结合内皮细胞和间叶干细胞,使其提供支撑作用并在立体水凝胶中形成血管。
而在该文献中,作者Daniel Nothdurfter等人将生物3D打印与流体芯片(Fluidic chip)相结合,开发了一种全新的灌注和微血管化的肿瘤微环境模型(Perfused and micro-vascularized tumorenvironment model)。在文章中,作者首先使用激光雕刻聚甲基丙烯酸甲酯(Polymethylmethacrylate,PMMA)薄片,使其中间具有一个圆形孔(模拟肿瘤微环境)、两侧各有两条槽(模拟血管);同时,使用regenHU生物3D打印机3DDiscovery BioSafety的细胞亲和性打印头以喷墨的方式将含有细胞的水凝胶均匀喷洒在孔及两侧血管槽内,以形成微环境的主体;为保证血管空腔的形成,作者也使用了牺牲材料Pluronic F-127——一种低温呈液态,高温呈凝胶状的材料——结合打印机的挤压式打印头,在凹槽内铺设血管。之后继续用含有细胞的水凝胶覆盖,降温使Pluronic F-127融化流出,即可得到具有空腔、可流经液体的血管结构(图1、图2)。
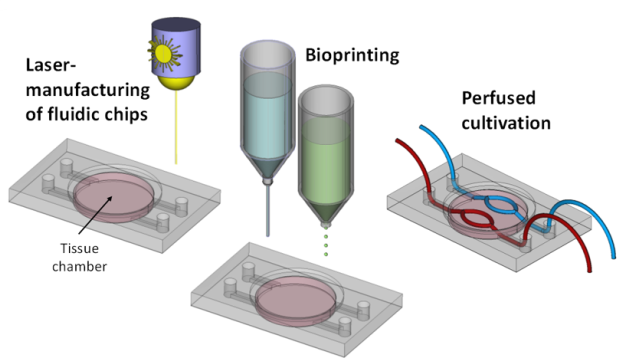
图1 文中提到的肿瘤微环境模型构建的三个步骤:激光雕刻流体芯片、生物墨水打印、形成可灌注的血管及肿瘤微环境

图2 左:打印Pluronic F-127后的模型;右:降温去除牺牲材料后,使用染色的PBS进行灌注的效果
根据该模型结构,作者尝试使用一种明胶-甲基丙烯酸酯(Gelatin-methacrylate,GelMA)与纤维蛋白(Fibrin)混合基质搭配多种类型的细胞,模拟肿瘤微环境;同时,通过添加内皮细胞,以促进微血管的自发形成。结果表明,脂肪细胞(Adipocyte)或诱导多能干细胞(Induced pluripotent stem cells,iPSCs)来源的间充质干细胞(Mesenchymal stem cells)都可以诱导肿瘤微环境的形成。另一方面,在去除牺牲材料的管状结构内表面涂上内皮细胞,可生长成致密的血管组织,形成组织屏障。
之后作者在打印过程中将患者来源的神经母细胞瘤球状体添加到基质里,并培养超过两周的时,成功展示了微血管被肿瘤球状体吸引并生长的过程(图3);而肿瘤球状体一旦破裂或无法维持球状,则肿瘤细胞会很快入侵周围的微环境(图4)。
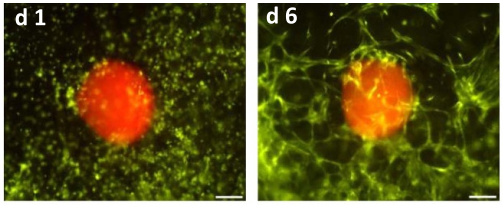
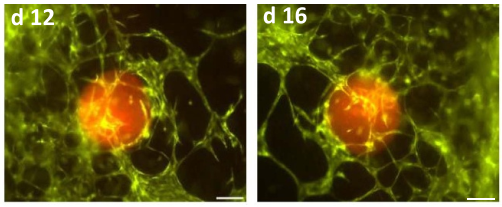
图3 添加了神经母细胞瘤球状体(红)的模型基质,分别在第1、6、12、16天的微血管(黄绿)生长情况(比例尺:200 μm)
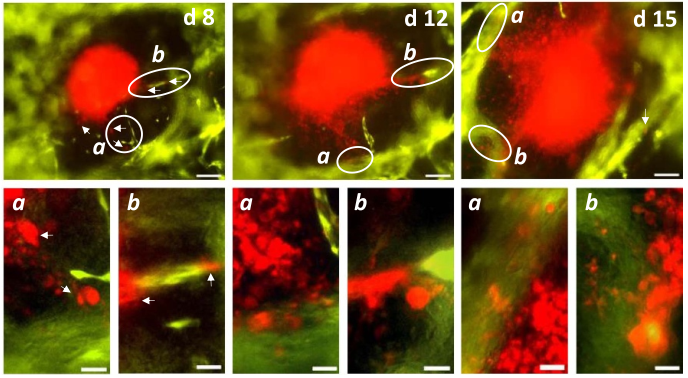
图4 肿瘤球状体(红)破裂后在微环境中的扩散情况(比例尺:第一行为200 μm;第二行为50 μm)
小结:该文献介绍了一种微血管化的神经母细胞瘤的肿瘤微环境模型,其特点在于通过生物3D打印,可进行高度定制;同时结合了流体芯片,使其结构更加稳定、统一,形成了一个中等通量的生物制造平台,有利于开展更为复杂、系统的实验,在未来医疗的肿瘤血管生成和转移研究中也能有很大的发挥余地。
新一代regenHU生物3D打印机保留上一代高精度、高稳定性优势的同时,提供更为简洁的模块化设计,可根据用户应用方向自行定制独特组合功能。设备整体专为生物打印考量,提供从料仓到打印平台全程的细胞生理温度和无菌环境。如需了解细节,请拨打联系电话:021-37827858 或 13818273779(微信同号)。
REGENHU生物3D打印机 R-GEN100 的样机已经到锘海啦!欢迎各位老师前来测样!

 从环境监测仪器上市企业财报看我国环境监测行业发展
从环境监测仪器上市企业财报看我国环境监测行业发展

 评论
评论