仪器社区
电解质溶液能够导电,遵守欧姆定律。在一定温度下,一定浓度的电解质溶液的电阻为

式中,R为电阻,Ω;ρ为电阻率,Ω·m;L为两个电极间的距离,cm;A为电极的面积,cm2。
电导定义为电阻的倒数,有
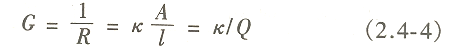
式中,G为电导,S;κ为电导率,S/cm,κ=1/ρ;Q为电导池常数,Q=L/A。
对电解质溶液的电导还与溶液中存在的离子的多少及性质有关。用摩尔电导的概念更能比较不同电解质溶液的电导能力。
摩尔电导是指相距1cm的两平行的大面积电极,放人含有1mol溶质的溶液的电导。有

式中,Am为摩尔电导率,S·m2/mol;cm为溶液中某物质的浓度,mol/L,需说明表示浓度的化学式单元,如NaCl、 ½K2S04、⅓LaCl3等 电解质的电导是由溶液内的正、负离子共同担的。强电解质的摩尔电导率是摩尔离子电导率的总和。
电解质的电导是由溶液内的正、负离子共同担的。强电解质的摩尔电导率是摩尔离子电导率的总和。有

式中,λ+、λ-分别为正、负离子的摩尔电导率。

式中,cmi为离子的摩尔浓度,mol/L;λi为离子的i摩尔电导率。
由于离子之间的相互作用,溶液的摩尔电导率随电解质浓度而改变。当溶液无限稀释时,λ+、λ-趋于极大值,用λ0+、λ0-表示,称为极限摩尔电导率。λ0表示离子在给定溶液无限稀释时的极限摩尔电导率,仅与温度有关,是各种电解质导电能力的特征常量。
离子的极限摩尔电导率的数据可用来计算电解质的极限摩尔电导率,以比较各种溶质的相对电导率,推断电导变化的趋势。

 评论
评论