利用ACE键合相的固定相选择
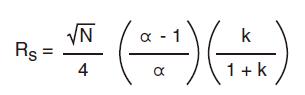
分离度方程式可以确定影响分离度的参数:柱效(N)、容量因子(k)和选择性(α)。
在过去几年里,柱效和使用超GX色谱柱(被称为“UHPLC”色谱柱)作为实现分离目标的手段已得到了极大的重视。
UHPLC已通过更快速的分离和更快速的方法开发提高实验室生产力来证明了其价值。
然而,选择性往往被忽视,且其重要性也被强调柱效所掩盖。这是令人遗憾的。
在影响分离度的三个参数中,选择性是Z为重要的。
(参见图1)通过利用柱效和选择性,通常可以实现更好和更快的分离。
图 1:N、α和k对分离度(Rs)的影响

提高N,α或k可以提高分离度(Rs)。
然而,从这些图中可以看出,随着N或k值的提高,对分离度的改善效果也逐渐降低。
另一方面,提高选择性(α)则没有这个问题,因此其成为开发分离方法时的Z佳优化变量。
在反相色谱中,固定相与分析物之间存在多种相互作用的机制,这可以用来实现分离。
这些相互作用机制包括:疏水性结合、π-π、氢键、偶极-偶极和形状选择性。
不同类型的键合相将提供其中一种或多种相互作用机制。表1列出了ACE键合相和每种可能的主要相互作用机制,这取决于分析物和流动相条件。
表1: 比较不同键合相的分离机制/相互作用
ACE 键合相 | 疏水性结合 | π–π | 氢键结合 | 偶极-偶极 | 形状选择性 |
C18 | 强 | 无 | 无 | 无 | 弱 |
C18-HL | 极强 | 无 | 无 | 无 | 弱 |
C18-AR | 强 | 强 | 中等 | 中等 | 中等 |
C18-PFP | 强 | 强 | 强 | 强 | 强 |
AQ | 中等 | 无 | 中等 | 弱 | 无 |
C8 | 中等 | 无 | 无 | 无 | 无 |
C4 | 弱 | 无 | 无 | 无 | 无 |
苯基 | 中等 | 强 | 弱 | 中等 | 弱 |
CN | 弱 | 无 | 弱 | 强 | 无 |
利用键合相的选择性实现更好的分离。
图2表明了两种ACE键合相即C18-AR与苯基之间的选择性差异。
尽管两种键合相提供了强π-π和偶极-偶极相互作用的可能性,但是在其它可能的相互作用机制(特别是疏水性结合)的强度方面,它们存在显著差异。
C18-AR可能具有其它不同的分离机制,可以为复杂的混合物带来更好的分离效果。对于其他混合物,可能不是这种情况,这是ACE键合相的优势。
当开发分离方法时,ACE键合相可以提供各种可供选择的重要保留机制。
非常强大且独特的C18-AR和C18-PFP相只有在ACE和ACE Excel色谱柱中可以获得。
通过利用柱效和选择性,可以实现更好的分离。
图 2:C18-AR与苯基相之间选择性差异的比较
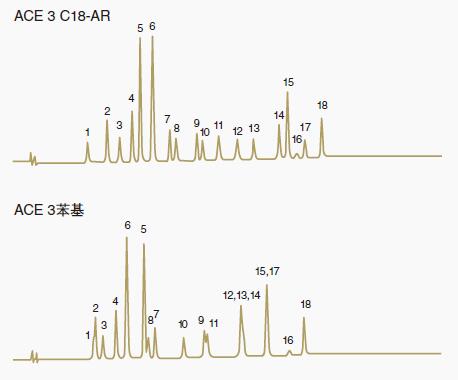
色谱柱尺寸: 50 x 2.1 mm, 3 μm
流动相:
A= 20mM KH2PO4,pH 2.7(溶于水中);
B= 20mM KH2PO4,pH 2.7(溶于甲醇/水中:65:35, v/v)
流速: 0.6 mL/min
温度: 60 ℃
检测: UV 214 nm
梯度: 5分钟内从3至B,并持续1分钟。
样品:
1. 甲硝唑
2. 3-羟基苯甲酸
3. 苯酚
4. 苯甲醇
5. 咖啡茵
6. 水杨酸
7. 喹喔啉
8. 苯甲酸
9. 奎宁
10. 非那西丁
11. 1,4-二硝基苯
12. 1,3,5-三硝基苯
13. 呋塞米
14. 1,3,5 -三甲氧基苯
15. 吡罗昔康
16. 卡维地洛
17. 苯甲酸乙酯
18. 去甲替林
C18-AR相的疏水性更大,这可以为色谱峰对(13,14)和(15,17)提供更多的保留值和更佳的选择性。还要注意C18-AR与苯基相的洗脱顺序有很多变化。
图3给出了键合相选择能力的另一实例。
一个分离是用C18键合相的UHPLC色谱柱完成,另一个分离是用C18-PFP键合相的UHPLC色谱柱完成。
C18-PFP键合相提供的额外分离机制,使得总体分离效果更佳出色。
图 3:ACE Excel可以获得zhuo越的分离度和峰形:药物及其相关物质的UHPLC结果
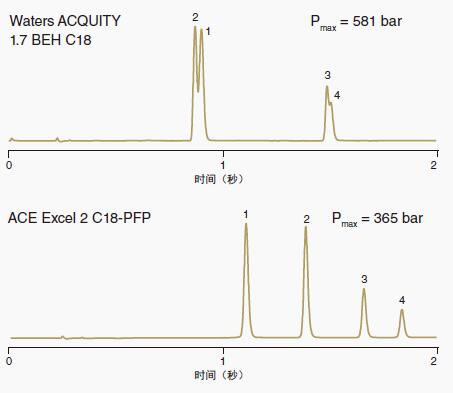
条件
色谱柱尺寸:50 x 2.1mm
流动相:
A = 5mM甲酸(溶于水中)
B = 5mM甲酸(溶于甲醇中)
梯度:5分钟内从3至B
流速:0.6 mL/min
温度:40 ℃
检测:UV 254 nm
样品
1. 对乙酰氨基酚
2. 氢氯噻嗪
3. 甲基苯基亚砜
4. 甲基苯砜
在C18 UHPLC色谱柱和C18-PFP色谱柱上同样快速地产生色谱图。
然而,C18-PFP色谱柱可以为色谱峰对(13,14)和(15,17)提供更佳的选择性,因此能够提供优越的总体分离性能。
 Z全的液相色谱柱知识分享和选择技巧,你值得拥有!参数、正反相对比、选择等一手
Z全的液相色谱柱知识分享和选择技巧,你值得拥有!参数、正反相对比、选择等一手
 气液相色谱柱保存小贴士:“我”也需要过个舒适年
气液相色谱柱保存小贴士:“我”也需要过个舒适年

 评论
评论