1.晶体场对称性的影响
根据
可以计算分裂后各组d 轨道的相对能量。前已指出假如一个ZX离子处于球形对称的负电场中,它的d 轨道能量会有所升高,但并不发生分裂,设其能量为E。
指出,不管晶体场的对称性如何,受外电场影响的d 轨道的平均能量保持不变。现选择球形对称中d 轨道的能量E=0,则在非球形对称性的晶体场中各d 轨道总能量的变化也为零。因此对于一个八面体场,以Δ(下标o代表八面体octahedral)或10Dq表示八面体场的分裂能。有下列关系。
E-E=Δ 2E+3E=0
令Δ=10Dq,解上述
,即得:
E=Δ=6Dq E=Δ=-4Dq
可见在八面体场中,d 轨道能级分裂结果与球形场中简并d 轨道能级E相比较,d轨道能量上升了6Dq,d轨道能量下降了4Dq。
在四面体场中,以Δ(下标t代表四面体 tetrahedral)表示四面体场的分裂能,
Δ=Δ,因为d 轨道受配体的排斥作用较八面体小,其d 轨道能量间的关系为:
E-E=Δ=Δ=×10Dq=4.45Dq
3E+2E=0
解上述
,即得:
E=-2.67Dq E=1.78Dq
现将八面体场、四面体场、平面四方形场中d 轨道能级分裂的相对数值(以Dq作单位)列在表7-5中,它们的相对关系见图7-9。
仅从
的几何构型看,分裂能Δ大小的顺序为:平面正方形>八面体>四面体
必须指出,这些能级图严格地讲只能用于1个d 电子的情况,多于1个d 电子的体系,因电子之间相互作用变得复杂,有时能级甚至颠倒。此外,更重要的是分裂能Δ仅占组成
的总结合能的一小部分(5%~10%)。例如[Ti(HO)]的Δ约为251.04kJ·mol,而Ti的水合能约为4184 kJ·mol。但是Δ的意义是很大的,它是晶体场的核心。
2.配体和ZX离子的影响
分裂能的大小除与晶体场对称性有关外,还和配体和ZX离子的性质有关,有下列规律:
(1)对同一ZX离子,Δ值随配体不同而变化,大致按下列顺序增加:
I<Br(0.76)<Cl(0.80)<-CN<F(0.9)~尿素<OH~--N=O(
根) ~HCOO
<CO(0.98)<HO(1.00)<-CS<EDTA<吡啶(1.25) ~NH<en(1.28)<SO
<联吡啶~
(1.34)<-O(硝基)<CN(1.5~3.0) ~CO
配位体下面划线的表示
。括号内的数字是以HO的Δ=1.00时的相对值。这个顺序称“光谱化学序”(spectro-chemical series),即配体场强度的顺序。它是从光谱实验中总结得到的。通常将Δ值大的配体如CN离子等称强场配体,而Δ值小的配体如I、Br离子等称弱场配体。从光谱化学序可粗略地看出,按
来说Δ值的大小为:
<氧<氮<碳。
下面列出某些
的
能Δ值,从中可看出配体场强弱的规律,见表7-6。
(2)对于相同的配体,同一金属原子高价离子的Δ值比低价离子大。如[Fe(HO)]和[Fe(HO)]的Δ值分别为13700cm 和10400cm。
(3)在配位体和
的氧化值相同时,Δ值按下列顺序增加:diyi过渡系<第二过渡系<第三过渡系。如Co、Rh、Ir的乙二胺配离子的Δ值分别为23300cm、34400cm、和41200cm。
由此可见Δ和Dq的值在不同的配合物中是不同的。分裂能Δ的值从实验测得,一般情况下其范围在10000~40000cm之间,处于可见和近紫外光区。


 【THUNDER小课堂】肿瘤细胞中有丝分裂纺锤体的成像
【THUNDER小课堂】肿瘤细胞中有丝分裂纺锤体的成像
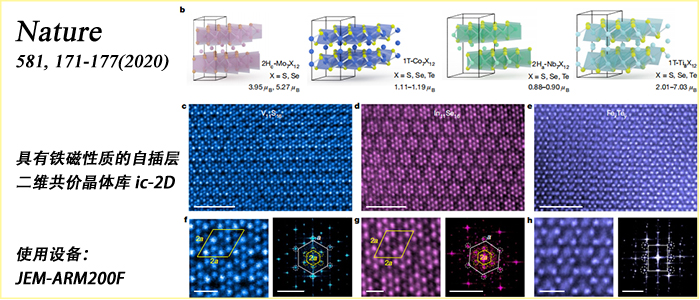 二维共价晶体库:原子自插层实现全新晶体结构及铁磁序
二维共价晶体库:原子自插层实现全新晶体结构及铁磁序

 评论
评论