克莱门森还原反应----阿拉丁试剂
2023-10-07262
克莱门森还原反应克莱门森还原反应简介
克莱门森反应 (Clemmensen Reduction)是指一种在浓盐酸溶液加热回流条件下,使用锌汞齐将醛或者酮中的羰基还原为亚甲基的有机化学反应。[1] 该反应是以其发现者丹麦裔美国化学家埃里克·克里斯蒂安·克莱门森(Erik Christian Clemmensen)的名字命名的。[2]
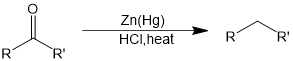
图1. 克莱门森还原反应
使用是克莱门森还原反应的条件在还原芳基烷基酮[3][4](例如在傅-克酰基化反应中的产物)此类使用场景下特别有效。因此,克莱门森还原反应与傅-克酰基化反应的配合合成烷基芳烃的经典策略。
克莱门森还原反应机理
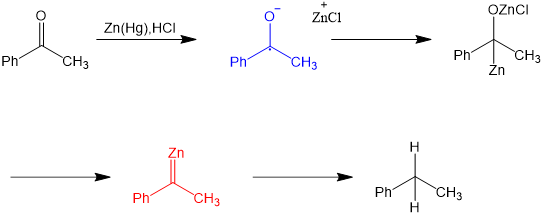
图2. 克莱门森还原反应机理
克莱门森还原反应机理于1975年提出。[5][6] 羰基首先转化为自由基阴离子(显示为蓝色),然后转化为锌类碳烯(显示为红色),然后还原为烷烃。
尽管该反应早在1914年就已被发现,但至今为止克莱门森还原反应机理仍然模糊不清。由于反应自身的非均相性质,使得反应机理研究的难度增加,只有少数研究被公开。[7,8] 目前的两种机理观点均涉及有机锌中间体,一种是碳阴离子机理,另一种则是类碳机理。Brewster提出了在金属表面发生还原反应的可能性。根据羰基化合物的结构或者反应的酸度,在化合物附着在金属表面后,形成碳-金属键或者氧-金属键。[7] 与此不同,Vedeja则是提出了一种首先形成自由基阴离子和锌碳化合物,然后再还原成烷烃的反应机理。[5,6](如上图所示)然而,醇和碳化物被认为不是中间产物,因此,即使的在克莱门森反应条件下,醇也难以得到烷烃产物。[7,9]
克莱门森反应应用
高度对称的碳氢化合物因其美观的结构和潜在的应用引起了科学家们的兴趣,但是在合成的过程中依然遇到了许多困难。Suzuki等人利用克莱门森还原反应合成了一种碳氢化合物——Dibarrelane。[10] 他们设定二级醇发生了SN1反应,形成了氯化物。然后,过量的锌还原氯化物。重要的是,该反应有效地还原了两个酮、醇和甲氧基羰基,同时还避免了副产物的生成,以高产率(61%)得到了目标产品。
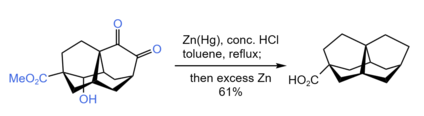
图3. Dibarrelane的合成[10]
克莱门森还原反应对脂肪族化合物和环状酮类化合物不是特别有效。一种优化后的反应条件,将活性锌粉和盐酸加入到乙 醚或乙酸酐的无水溶液中,可以提高还原反应的效率。此外,优化后的克莱门森还原反应还可以对含有稳定基团(如氰基、氨基、乙酰氧基和烷氧羰基)的分子中的酮基进行选择性脱氧。Yamamura等人使用优化后的克莱门森反应条件有效地将胆甾烷-3-酮还原成胆甾烷,并以高产率(约76%)得到了目标产品[11]。
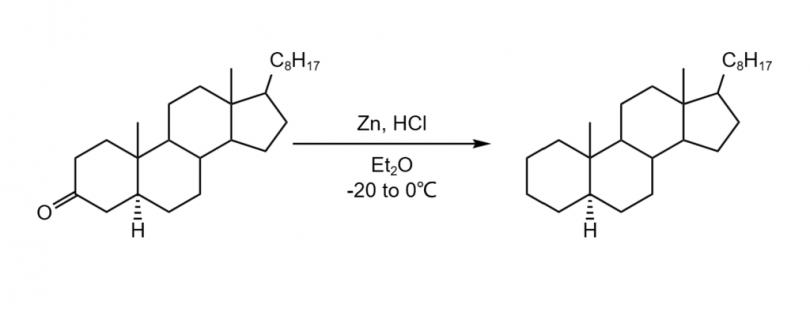
图4. 使用克莱门森还原反应将胆甾烷-3-酮还原为胆甾烷[11]。
克莱门森反应的局限性及解决方案
要想使用克莱门森还原反应,那么底物需要可以承受反应的强酸性条件(37% HCl)。有以下两种解决方案可供选择。Wolff-Kishner还原反应可以还原在强碱条件下稳定的酸敏性底物;而在雷尼镍条件下对氢解稳定的底物,可以通过Mozingo还原反应制得缩硫醛或缩硫酮,再用雷尼镍进行还原。
参考文献
1. Smith, Michael (2007). March's advanced organic chemistry : reactions, mechanisms, and structure. Jerry March (6th ed.). Hoboken, N.J.: Wiley-Interscience.
2. Clemmensen, Erik (1913). "Reduktion von Ketonen und Aldehyden zu den entsprechenden Kohlenwasserstoffen unter Anwendung von amalgamiertem Zink und Salzsäure". Berichte der deutschen chemischen Gesellschaft. 46 (2): 1837–1843. https://doi.org/10.1002/cber.19130460292\
3. "Y-PHENYLBUTYRIC ACID". Organic Syntheses. 15: 64. 1935. https://doi.org/10.15227/orgsyn.015.0064
4. "CREOSOL". Organic Syntheses. 33: 17. 1953. https://doi.org/10.15227/orgsyn.033.0017
5. Li, Jie Jack (2021), Li, Jie Jack (ed.), "Clemmensen Reduction", Name Reactions: A Collection of Detailed Mechanisms and Synthetic Applications, Cham: Springer International Publishing, pp. 109–111, https://doi.org/10.1007/978-3-030-50865-4_31
6. Vedejs, E. (1975), John Wiley & Sons, Inc. (ed.), "Clemmensen Reduction of Ketones in Anhydrous Organic Solvents", Organic Reactions, Hoboken, NJ, USA: John Wiley & Sons, Inc., pp. 401–422, https://doi.org/10.1002/0471264180.or022.03
7. Brewster, James H. (1954). "Reductions at Metal Surfaces. II. A Mechanism for the Clemmensen Reduction 1". Journal of the American Chemical Society. 76 (24): 6364–6368. https://doi.org/10.1021/ja01653a035
8. Nakabayashi, Tadaaki (1960). "Studies on the Mechanism of Clemmensen Reduction. I. The Kinetics of Clemmensen Reduction of p-Hydroxyacetophenone". Journal of the American Chemical Society. 82 (15): 3900–3906. https://doi.org/10.1021/ja01500a029
9. Martin, Elmore L. (2011), John Wiley & Sons, Inc. (ed.), "The Clemmensen Reduction", Organic Reactions, Hoboken, NJ, USA: John Wiley & Sons, Inc., pp. 155–209, https://doi.org/10.1002/0471264180.or001.07
10. Suzuki, Takahiro; Okuyama, Hiroshi; Takano, Atsuhiro; Suzuki, Shinya; Shimizu, Isao; Kobayashi, Susumu (2014-03-21). "Synthesis of Dibarrelane, a Dibicyclo[2.2.2]octane Hydrocarbon". The Journal of Organic Chemistry. 79 (6): 2803–2808. https://doi.org/10.1021/jo5003455
11. "MODIFIED CLEMMENSEN REDUCTION: CHOLESTANE". Organic Syntheses. 53: 86. 1973. https://doi.org/10.15227/orgsyn.053.0086.
阿拉丁提供相关产品,详情请见阿拉丁官网:Clemmensen Reduction (aladdin-e.com)



