Cell:肿瘤组织中ECM硬度如何加剧CD8+ T细胞耗竭
厦门大学细胞应激生物学国家重点实验室 周大旺教授、陈兰芬教授
导言
细胞外基质(ECM)的结构与硬度变化一直是癌症中具有代表性的特征。而ECM的生物力学性质的变化真正如何影响肿瘤反应性CD8+ T细胞仍旧是悬而未决的问题。来自厦门大学细胞应激生物学国家重点实验室的周大旺教授、陈兰芬教授等研究组最近在Cell杂志上发表的最新研究结果揭示了转录因子Osr2是如何整合生物力学信号并促进肿瘤反应性CD8+ T细胞耗竭 (Zhang et al. Cell, 2024)。
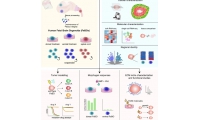
肿瘤微环境中被基质包围的T细胞在较软的ECM中会有更高的细胞迁移能力与免疫检查阻断肿瘤疗效增强。通常实体瘤(Solid Tumor)中的ECM相较于正常组织会具有更大的硬度,而这种硬度的增加被发现与肿瘤中的CD8+ T 细胞耗竭现象存在关联。为了探索这一现象的机理,本文作者首先使用生物型原子力显微镜 NanoWizard 4对人类肝细胞癌(HCC)组织进行Collage I免疫荧光染色与组织硬度的原位测量。测量结果(图一A)显示,HCC组织中Collage I高表达区域的硬度更高。此外,Collage I高表达亦伴随着更高水平的PD-1与 TIM-3,显示该区域内有大量晚期耗竭的CD8+ T细胞(图一 B&C)。为了验证CD8+ T细胞耗竭与ECM硬度刺激的相关性,研究者建立了一套体外细胞培养模型:在T细胞受体激活48小时后使用不同硬度(5、40 、200 kPa,AFM测定)的PDMS Gel来诱导CD8+ T细胞耗竭。实验证实,模拟更高ECM环境硬度的PDMS Gel,会显著提高 CD8+ T细胞耗竭。
图一 机械力增强CD8+ T细胞耗竭
在确立肿瘤组织中ECM硬度和CD8+ T细胞的关联后,研究者们进一步探索了与此现象相关的细胞机械力受体与其下游调控的信号通路。根据体外细胞培养模型结果(图二),硬的PDMS Gel会激活机械力离子通道Piezo 1,提高胞内钙离子浓度。而使用Piezo 1的抑制剂 GsMTx4或Pizeo 1敲除会明显改善和逆转CD8+ T细胞耗竭趋势。
图二 机械力离子通道Piezo 1 的钙离子内流诱导CD8+ T细胞耗竭
确定了导致CD8+ T细胞耗竭的机械力受体为Piezo 1后,研究者们继续使用Piezo 1的激活剂Yoda 1来探索下游的信号通路。根据RNAseq结果,Osr2 转录因子在CD8+ T细胞上Piezo 1被激活后,其表达量显著提高(图三)。一系列生化实验结果表明,Osr2的表达是通过耦合T细胞受体(TCR)信号和Piezo1/CaMKII/CREB轴介导的生物力学应激信号,在终末枯竭的肿瘤特异性CD8+ T细胞亚群中进行选择性诱导。基于此,敲除Osr2亦被证明可降低CD8+ T细胞耗竭并显著提高CAR-T治疗效果(图三)。
图三
Osr2在受机械应力激活的CD8+T细胞中选择性诱导
机械应力通过Piezo1/CaMKII/CREB/Osr2轴增强CD8+ T细胞枯竭
Osr2特异性减弱终末枯竭的CD8+T细胞的功能靶向Osr2信号增强T细胞介导的固体肿瘤免疫疗法
(实验细节与结果请参见原文)
所推广产品图片/官网链接:
网址链接:https://doi.org/10.1016/j.cell.2024.04.023
布鲁克生物型原子力显微镜NanoWizard? V: 精确的生物力学定量工具,可与各种高级荧光显微镜结合,对生物分子、病毒、细菌、细胞和组织进行形貌、力学与荧光信号等多通道原位测量。
推荐人:曹旭 部 应用科学家
全部评论(0条)
推荐阅读
-
- Cell:肿瘤组织中ECM硬度如何加剧CD8+ T细胞耗竭
- 肿瘤微环境中被基质包围的T细胞在较软的ECM中会有更高的细胞迁移能力与免疫检查阻断肿瘤疗效增强。
-
- 【案例研究】肿瘤组织中肿瘤和免疫细胞的空间结构
- 【案例研究】肿瘤组织中肿瘤和免疫细胞的空间结构
-

- 树突状细胞肿瘤疫苗中RNA修饰机制研究进展
- 近年来,树突状细胞(DC)肿瘤疫苗在免疫治疗领域展现出重要潜力。本研究聚焦RNA修饰技术对DC疫苗功能的影响,通过优化RNA转染效率及稳定性,探索其激活抗肿瘤免疫的分子机制。
-
- Cell重磅:人脑类器官直接由人类胎儿脑组织产生
- 大脑是人体最复杂的器官,数百年来解释大脑发育和神经系统基本的机制一直是科学研究中令人着迷的挑战。科学家通过建立细胞或动物模型来进行体内或体外研究,提高了人们对人脑生理和病理的认知。
-
- 团聚细胞计数的应用解决方案:Cell Type参数优化
- 团聚细胞计数的应用解决方案:Cell Type参数优化
-
- 团聚细胞计数的应用解决方案:Cell Type参数优化
- 团聚细胞计数的应用解决方案:Cell Type参数优化
-

- 阳离子脂质体介导肿瘤细胞基因转染研究
- 阳离子脂质体在肿瘤细胞基因转染中的应用,通过构建高效的基因转染体系,详细探讨了不同脂质体配方、转染条件对转染效率的影响。实验结果显示,优化的阳离子脂质体配方能显著提高肿瘤细胞的基因转染效率。
-
- 新鲜出炉!超速离心如何助力肿瘤研究?
- 4小时提取高纯度TEVs,肿瘤研究中的高效方法
-
- Nature Materials: 细胞翻滚 (Cell Tumbling) 通过细胞核机械转导增强水凝胶中干细胞的分化
- 力学刺激是导致细胞环境改变的重要物理因素,在力学信号转导的过程中,各种信号通路作为细胞行为的调节器,调控细胞的增殖,分化和凋亡。
-
- 案例 | 生产制造中的硬度评价
- 生活中我们不仅需要评价产品的外观尺寸,还需要对硬度等物理性状加以分析。作为一种评价材料软硬的重要指标——硬度,遍布在我们的生活之中。
①本文由仪器网入驻的作者或注册的会员撰写并发布,观点仅代表作者本人,不代表仪器网立场。若内容侵犯到您的合法权益,请及时告诉,我们立即通知作者,并马上删除。
②凡本网注明"来源:仪器网"的所有作品,版权均属于仪器网,转载时须经本网同意,并请注明仪器网(www.yiqi.com)。
③本网转载并注明来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
④若本站内容侵犯到您的合法权益,请及时告诉,我们马上修改或删除。邮箱:hezou_yiqi





















参与评论
登录后参与评论