
立即扫码咨询
联系方式:400-099-8212
联系我们时请说明在仪器网(www.yiqi.com)上看到的!
【概述】
近年来基因毒性杂质成为人们关注的焦点,甲磺酸酯、苯甲磺酸等磺酸类物质与微量的低级醇在合成反应中生成烷基磺酸如甲磺酸甲酯(MMS)、甲磺酸乙酯(EMS)、异丙基甲磺酸酯(IMS)、正丁基甲磺酸酯(NBMS),以及芳基磺酸酯如苯磺酸甲酯(MBS)、苯磺酸乙酯(EBS)、对甲苯磺酸酯(MP-TS),这些物质可与DNA发生烷基化反应,从而可能成为引发癌症的诱因,因此控制药物中该类杂质的毒理学关注阈值(TTC)水平非常重要,欧洲医药评价署(EMEA)发布了关于基因毒性杂质的Zda摄取量为1.5μg/d。这些潜在基因毒性的存在引起管理机构的高度重视,为防止奈非那韦事件的发生,EMEA首先实施详细指南控制杂质限度,美国食品和药物管理局(FDA)随后颁布指南草案,国际药品注册协调会议(ICH)也对基因毒性杂质做出限度规定,《欧洲药典》增补版7.3明确指出采用衍生化法检测药物中MMS、EMS、IMS(2.5.38)。
甲磺酸酯基的存在可以使C—O键之间变的活泼,发生断裂后生成碳正离子而具有烷化作用。基于对此认识,人们开始研究磺酸酯类化合物,希望找到有效的抗肿瘤药物,从中发现了白消安(Busulfan,马利兰),其结构中含有2个甲磺酸基团,为双功能的烷化剂,可以与DNA中的鸟嘌呤集合,产生分子内交联,从而使肿瘤细胞死亡。临床上对慢性粒细胞白血病的LX显著,主要的不良反应为消化道反应及骨 髓YZ。
目前因基因毒性物质的概念广泛,所含种类繁多,对于磺酸酯类的物质除去其治癌作用外,其它的性质尚未探知,而其致癌致畸的作用却是不可否认的。对于欧洲药典中采用衍生化法测定MMS、EMS、IMS,如果某药品中含有甲基、乙基、异丙基类物质,则该方法不可避免的存在其测定局限性,本方法主要提出了一种采用液体直接进样法分析药物中8种磺酸酯的GCMS方法,方法快速、有效,灵敏度满足对微量分析的要求。
【实验/设备条件】
仪器方法
进样口温度:250℃;
进样模式:splitless,
不分流时间:1min;
进样体积:1μL,
载气:氦气,1.0 mL/min
柱温:50℃(1 min),10℃/min到280℃(5 min)
离子源:温度280℃,Transfer line : 280℃
扫描方式:SIM模式
【实验/操作方法】
溶液配制
标准溶液:0.05 g 8种磺酸酯于50 mL乙酸乙酯定溶制得标准储备液。
标准工作液:取以上标准储备液稀释至0.01μg/mL、0.02μg/mL、0.05μg/mL、0.1μg/mL、0.2μg/mL、0.5μg/mL。
样品的前处理
提取:
可溶于有机溶液药品:称取某药品0.05 g于试管中,准确加入2 mL乙酸乙酯充分振荡,超声提取10 min。
水溶性药品:称取某药品0.05 g于试管中,准确加入2 mL甲醇:水(5 : 1)充分振荡,超声提取10 min,再以2 mL乙酸乙酯充分超声提取,过无水硫酸钠,以55℃氮吹致尽干,以2 mL乙酸乙酯定容。将以上处理液,过滤膜上GCMS分析。
加标样品的制备
将药品研磨制成粉末,称取该药品0.5 g,加入40μL的10μg/mL、250μg/mL标准稀释液,混均,制得含8种磺酸酯0.8μg/g、20μg/g的加标样品。
【实验结果/结论】
1.色谱柱的选择
磺酸酯类属于极性物质,易溶于水,在水存在下高温条件易发生分解反应,本方法根据极性首先选择极性色谱柱分析。本方法中考察了Tg-Wax MS 30 m×0.25μm×0.25 mm和Tg-35 MS 30 m×0.25μm×0.25 mm,Tg-5 MS 30 m×0.25μm×0.25 mm三种极性不同的色谱柱。因本方法选择液体直接进样,同时由于药品基质的复杂多样性极易导致较多的杂质进入色谱柱,如果长时间低温下做样会导致色谱柱的污染。另外方法中甲苯磺酸酯类沸点较高,也不易选择极性色谱柱。
当选择中等极性、非极性色谱柱时,实验结果表明,选择-5色谱柱分离效果较差,对甲苯磺酸甲酯、乙酯、异丙酯无法完全分离。
2.提取溶剂的选择
磺酸酯为药物生产中的副产物,本方法选择某样品测定,主要考察了乙酸乙酯、甲醇、乙腈、正己烷四种不同的溶剂的提取效率。对于可溶于有机溶剂的药品,当采用甲醇、乙腈做提取溶剂时,对药品中8种磺酸酯的提取效率也较好,由于甲醇、乙腈极性溶剂对色谱柱的损伤大,易导致色谱柱流失,因此本方法采用乙酸乙酯做为提取溶剂。
部分药品为水溶性药品,且其仅在水中溶解性较好,此时针对这些药品,本方法主要采用通过甲醇-水溶液进行提取(5 : 1),同时由于甲基磺酸甲酯、苯磺酸乙酯为微溶于水的,若直接以甲醇-水超声提取后过无水硫酸钠,该方法下此两种物质的回收率会受到影响,通过甲醇-水溶液(5 : 1)提取后,再以2 mL的乙酸乙酯进一步超声提取,可以达到更好的提取回收效率。
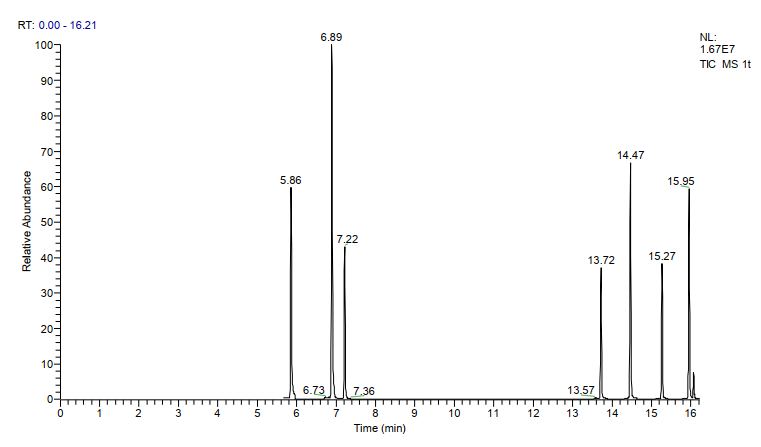
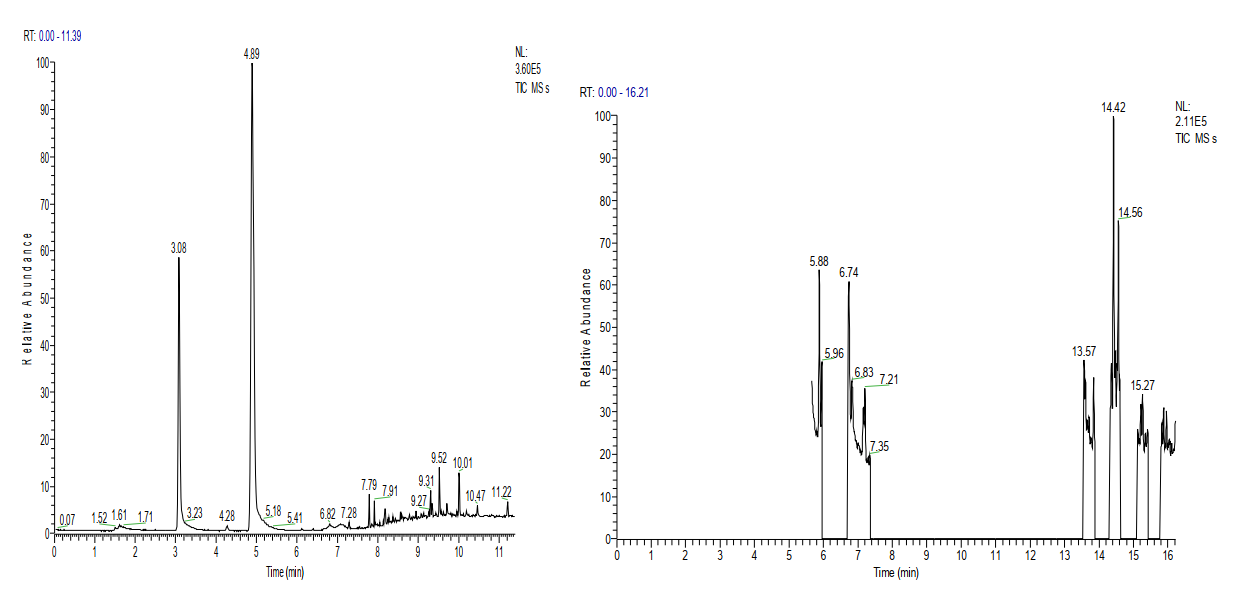
图1. 1μg/mL 8种磺酸酯的T-SIM扫描图。
3.标准品色谱图及样品加标色谱
磺酸酯为药物生产中的副产物,本方法的分析目标物及其定性、定量离子如下表1。本方法选择某样品测定,其中未含有8种磺酸酯,且该药品中无其它物质对所分析物质干扰,如下图2为空白、某样品及其加标色谱图。
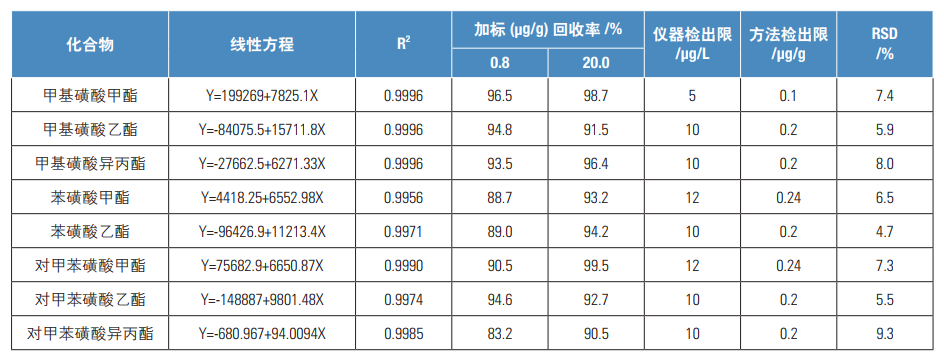
4.线性、检出限及RSD
配制浓度分别为:10.0、20.0、50.0、100.0、200、500μg/L的校准溶液,采用上述方法分别进样分析,考察各组分在10.0-500μg/L浓度范围内的线性。实验结果表明8种组分在10.0-500.0μg/L线性关系良好,线性相关系数均大0.995(见表2)。
对某样品添加混合标准溶液(加标浓度为0.8μg/g、20μg/g),考察8种磺酸酯的加标回收情况。实验结果表明各组分的加标回收率均在83.2-99.5%之间,符合日常分析检测的要求。对0.8、20μg/g加标水平平行测定6次,平均RSD值在4.7-9.3%,符合稳定性要求。同时以三倍信噪比计算各组分检出限,各组分仪器检出限在5.0-12.0μg/L(见表3)。
本方法能够满足欧洲药典中对甲基磺酸甲酯、乙酯、异丙酯的限量要求,同时对于其它5种磺酸酯也可以做0.24μg/g。
表1.分析物保留时间及定性定量离子
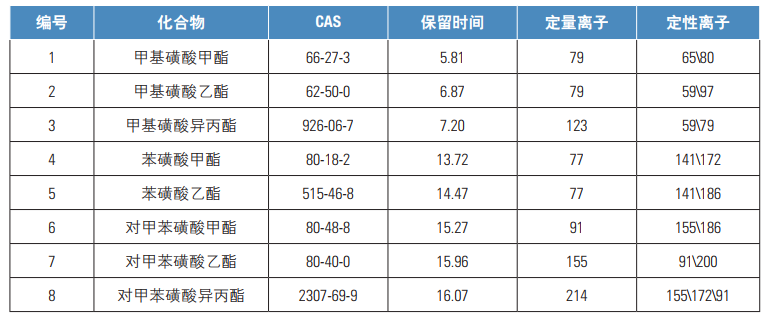
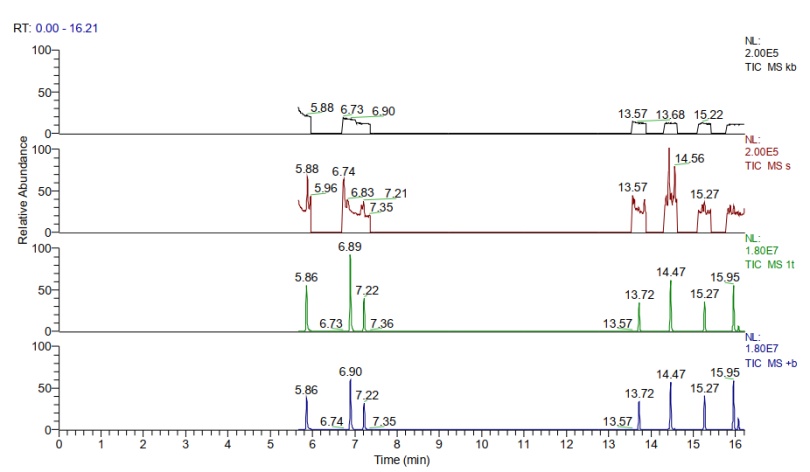
图2.空白、样品、标准品、样品加标浓度为20μg/g的TIC图,由上而下分别为空白、样品、标准品、样品加标
表3.线性、检出限及RSD数据(n=6)
5.方法的优势
在EP的方法中对于甲磺酸甲酯(MMS)、甲磺酸乙酯(EMS)、异丙基甲磺酸酯(IMS)采用衍生化法得到碘甲 烷、碘乙烷、碘异丙烷通过顶空方式进行分析衍生产物来对原药品中MMSEMSIMS的量此方法存在一定的局限性当药物中含有易与碘形成碘代烷的其他类型化合物时造成假阳性如下图某药品中并未检出甲基磺酸酯采用EP方法测得其中含中甲基磺酸乙酯(0.8μg/g)、异丙酯(2.6μg/g),均已超过本方法的定量限,因药品中可能含有某种乙基、异丙基化合物而使其测得结果含有碘乙烷、碘异丙烷。另外对于EP方法中采用顶空衍生法,其衍生过程需配制衍生化试剂进行衍生,过程繁多复杂,易造成偏差。本方法采用液体法直接进样法,前处理简单也是此方法的一个优势。
结论
本实验采用赛默飞世尔科技Trace1300GC配ISQ质谱检测器分析药品中的8种基因毒性物质——磺酸酯,样品通过乙酸乙酯超声提取可以完成药品中磺酸酯的萃取。同时对于EP方法中提出的顶空衍生化方法,其本身存在一定的局性限,本方法通过直接进样分析目标物,可以去除假阳性的影响,满足检测要求,本方法准确,灵敏度高。
【仪器/耗材清单】
仪器
• TraceFinder 3.2
• Thermo ScientificTM Trace 1310-ISQ, SSL进样口, AS1310自动
进样器
•色谱柱:TG-35 MS, 30 m, 0.25 mm, 0.25μm P/N: 26094-1420;
S/N: 1082682
•进样针:10μL
试剂与标准品耗材
HPLC级乙酸乙酯、甲醇、无水硫酸钠、8种甲基磺酸酯标准品。
【参考文献】
[1]张园园,李银峰,王杰晶乖.药物中痕量磺酸酯类物质的检测技术研究进展药物评价研究,2012,35 (4): 304-208.
[2] Graham E.Taylor, Mark Gos领, Andrea Pearce Low level determination of p-toluensulfonate and benzenesulfonate estersin drug substance by high performance liquid chromatograpy/mass spectormetry.2006, (1119):231-237
[3] Roberto Alzaga , Robert W. Ryanb. A generic approach for the determination of residues of alkylating agents in activepharmaceutical ingredients by in situ derivatization–headspace–gas chromatography–mass spectrometry.2007, (45):472-479
[4] European Pharmacopoeia 8.0.2.5.38,MMS,EMS and IMS in active substances
相关产品
全部评论(0条)
推荐方案
参与评论
登录后参与评论