| 行业应用: | 制药/化妆品 综合 |
【概述】
近年来基因毒性杂质成为人们关注的焦点,甲磺酸酯、苯甲磺酸等磺酸类物质与微量的低级醇在合成反应中生成烷基磺酸如甲磺酸甲酯(MMS)、甲磺酸乙酯(EMS)、异丙基甲磺酸酯(IMS)、正丁基甲磺酸酯(NBMS),以及芳基磺酸酯如苯磺酸甲酯(MBS)、苯磺酸乙酯(EBS)、对甲苯磺酸酯(MP-TS),这些物质可与DNA发生烷基化反应,从而可能成为引发癌症的诱因,因此控制药物中该类杂质的毒理学关注阈值(TTC)水平非常重要,欧洲医药评价署(EMEA)发布了关于基因毒性杂质的Zda摄取量为1.5μg/d。这些潜在基因毒性的存在引起管理机构的高度重视],为防止奈非那韦事件的发生,EMEA首先实施详细指南控制杂质限度,美国食品和药物管理局(FDA)随后颁布指南草案,国际药品注册协调会议(ICH)也对基因毒性杂质做出限度规定,《欧洲药典》增补版7.3明确指出采用衍生化法检测药物中MMS、EMS、IMS(2.5.38)。本文简要介绍了近年来磺酸酯类杂质检测方法的研究进展,探讨了不同检测方法的特点及不足;同时说明了杂质产生条件和避免该类杂质产生的具体措施,从而有效地控制杂质限度。
【实验/设备条件】
表1.仪器参数设置
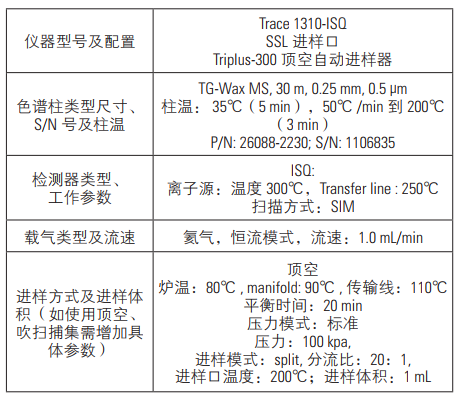
表2.分析物保留时间及定性定量离子
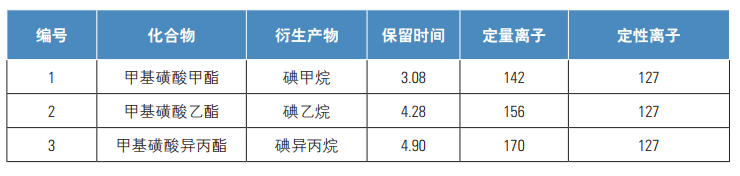
【实验/操作方法】
溶液配制
标准溶液:取本品30 mg溶于10mL甲苯溶液中,取50μL置于容量瓶中采用80%乙腈水溶液稀释至25mL,做为标准储备液A。
准确称取60g NaI+30 mg硫代硫酸钠溶于50mL水中,做为衍生化试剂B。
将A稀释至不同浓度的甲基磺酸酯1mL待用。
取以上0.5 mL甲基磺酸酯待用液+0.5mL衍生化试剂B于20mL顶空瓶中,待分析。
样品的前处理
称取某样品50 mg,溶于0.5 mL 80%乙腈水溶液,加入0.5mLNaI溶液于顶空瓶中,待上机分析。
【实验结果/结论】
顶空条件的选择
本实验选取80%乙腈水溶液做溶剂,可将待分析药品完全溶解,溶剂中含大量有机溶剂因此顶空温度不易过高,同时随着样品平衡温度的升高,进入气相的有机物的量增加,从而可以提高分析的灵敏度,但当孵化温度过高时,对分析目标物碘代烷的灵敏度有影响,从而降低气相中目标化合物的相对浓度,本实验中主要考察了40℃、60℃、80℃的平衡温度对灵敏度的影响,试验结果表明选择平衡温度80℃时目标化合物的灵敏度Zda,更适宜分析。实验中传输线温度选择110℃以保证没有水气带入色谱柱,影响分析效果。
当孵化时间增长分析物在水相和气相两相中的分配系数越小,当孵化时间达到一定时间分析物在两相间达到Zda的分配,此时为**的分析时间,本实验中考察了10 min,20 min,30 min,40 min,50 min,对孵化效率的影响,实验Z终结果表明,当孵化时间为20 min时效率Z高。如下图为不同孵化时间下孵化效率的比较图。
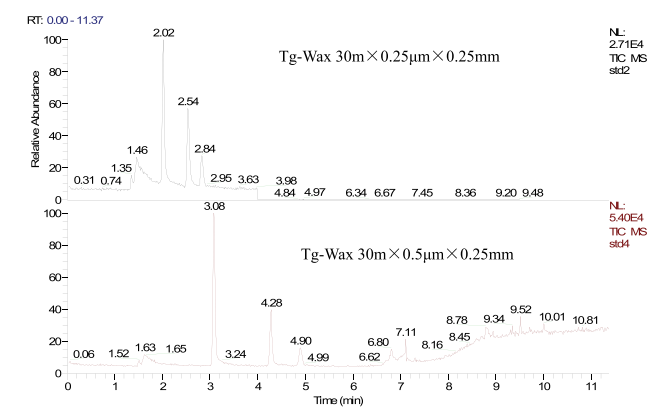
图1. 15μg/L甲基磺酸酯衍生后在不同膜厚Wax色谱柱上的分离情况
色谱柱的选择
参考欧洲药典8.0中对药品中甲基磺酸酯的分析测定方法,符合药品中基因毒性物质限量要求。本方法采用NaI衍生法将甲基磺酸酯衍生为碘 甲烷、碘乙烷、碘异丙烷,通过顶空法进行分析测定。分析的目标化合物碘 甲烷、碘乙烷、碘异丙烷为极性低沸点化合物,因此采用极性色谱柱,本方法中考察了Tg-Wax 30 m×0.25μm×0.25 mm和Tg-Wax 30m×0.5μm×0.25 mm两种不同膜后色谱柱,实验结果发现,当选择膜厚为0.25μm的色谱柱时,由于衍生产物沸点低,在色谱柱上保留能力较小,需将初始温度降到30℃低温,此时色谱峰形较差,有托尾现象。
当选择0.5μm色谱柱时,色谱峰拖尾得到改善,同时出峰时间推后,可将初始温度升至35℃。如下图为两种色谱柱下分析物的色谱图。
标准品色谱图及样品加标色谱
甲基磺酸酯为药物生产中的副产物,本方法选择某样品测定,发现其中含有甲基甲磺酸酯、甲基异丙基磺酸酯,某药品中无其它物质对所分析物质干扰,如图2为某样品及其加标色谱图。其中下图为样品加标色谱图。
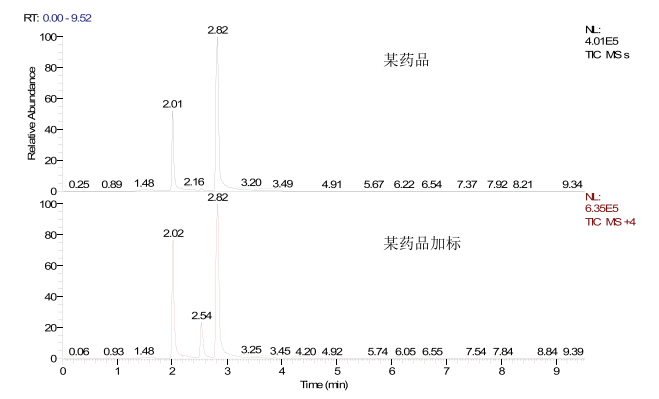
图2.图为加标1.5μg/g浓度样品加标、样品色谱图,其中2.01为甲基磺酸甲酯,2.54为甲基磺酸乙酯,2.82为甲基磺酸异丙酯
线性、检出限及RSD
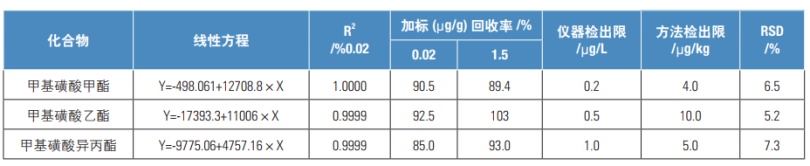
配制浓度分别为:1.0、5.0、15.0、75.0、150μg/L的校准溶液,采用上述方法分别进样分析,考察各组分在1.0-150μg/L浓度范围内的线性。实验结果表明3种组分在1.0-150μg/L线性关系良好,线性相关系数均大于0.999(见表3)。
对某样品添加混合标准溶液(加标浓度为0.02μg/g、1.5μg/g),考察三种甲基磺酸酯的加标回收情况。实验结果表明各组分的加标回收率均在85.0-103%之间,符合日常分析检测的要求。对0.02、1.5μg/g加标水平平行测定6次,平均RSD值在5.2-7.3%,符合稳定性要求。
同时以三倍信噪比计算各组分检出限,各组分仪器检出限在0.2-1.0μg/L(见表3)。
表3.线性、检出限及RSD数据(n=3)
结论
本实验采用赛默飞世尔科技Triplus 300顶空自动进样器结合1300GC配ISQ质谱检测器分析药品中的3种基因毒性物质——甲基磺酸酯,样品通过衍生法采用顶空进样方式,方法准确,灵敏度高,满足检测要求。
【仪器/耗材清单】
仪器:Trace 1310-ISQ SSL进样口 Triplus-300顶空自动进样器
色谱柱:TG-Wax MS, 30 m, 0.25 mm, 0.5μm
【参考文献】
[1]张园园,李银峰,王杰晶乖.药物中痕量磺酸酯类物质的检测技术研究进展药物评价研究,2012,35 (4): 304-208.
[2] Graham E.Taylor, Mark Gos领, Andrea Pearce Low level determination of p-toluensulfonate and benzenesulfonate estersin drug substance by high performance liquid chromatograpy/mass spectormetry.2006, (1119):231-237
[3] Roberto Alzaga , Robert W. Ryanb. A generic approach for the determination of residues of alkylating agents in activepharmaceutical ingredients by in situ derivatization–headspace–gas chromatography–mass spectrometry.2007, (45):472-479
[4] European Pharmacopoeia 8.0.2.5.38,MMS,EMS and IMS in active substances


赛默飞色谱与质谱中国
仪器网(yiqi.com)--仪器行业网络宣传传媒