| 行业应用: | 仪器仪表 仪器仪表 |
介绍
一次性系统(SUS)在制药和生物制药行业的使用继续增长。随着SUS产品的使用越来越多,对一次性组件的纯度问题及其对高价值Z 终产品的生物制造,储存和运输的潜在影响给予了更多的关注。Aramus™一次性冻存袋组件由单层、高等级、gamma稳定的含氟聚合物制成,可提供高纯度、极低的可萃取和可浸出(E&I)特性,出色的化学相容性以及提高关键工艺流体和Z 终产品的安全性。并且在通过ISO标准的5级洁净室制造,进行严格质量控制(QC),采用AccusSizer液体颗粒计数器进行污染颗粒检测。
关注颗粒物含量的原因1
⚫ 可能引起微小血管阻塞给患者带来风险
⚫ 干扰细胞生长
⚫ 药品质量、毒性和安全性
⚫ 干扰加工
出于这些原因,冻存袋的制造采用Z高的清洁度工艺,并进行了微粒污染测试。由于Entegris同时生产用聚酰胺含氟聚合物冻存袋组件和于质量控制测试的AccuSizer液体颗粒计数器,因此,通过严格的污染颗粒检测和质量把控,可以Z大限度地减少一次性组件系统颗粒污染。Aramus冻存袋的亚可见颗粒测试基于USP<788>标准2,并在其他Entegris应用说明中有详细记录3,4。这些测试的重点是在于USP<788>标准规定值,即大于等于10µm的微粒含量小于25颗/mL,大于等于25µm的微粒含量小于3颗/mL。所有测试的冻存袋100%符合USP<788>标准。
mRNA包裹脂质纳米粒的吸附研究
Entegris 与 Precision Nanosystems Inc.(PNI)5合作使用 lipid nanoparticles(LNPs)进行了一项mRNA包封研究,以比较Aramus氟聚物袋与常用玻璃瓶和聚丙烯(PP)冷冻管在七天储存时间内对mRNA-encapsulated LNP的材料吸附。在不同条件下培养后,评估mRNA-encapsulated LNPs溶液的理化特性,以建立与这三种密封材料接触的mRNA-LNPs稳定性的初始数据。使用PNI专有的脂质混合物和制剂系统配制模型mRNA(EPO)并将其封装到LNP中,等分到室温下储存的外壳中,然后在不同的时间点,即配制后的时间零点(T0)、24小时后和168小时储存后分析mRNA-LNP浓度,如图1所示,mRNA浓度见图2,mRNA-LNP平均粒径见图3。

图1 LNP浓度与时间的关系
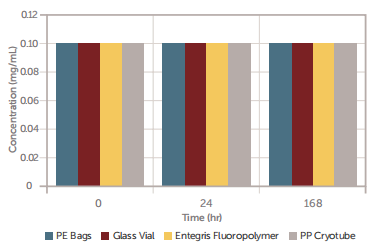
图2 mRNA浓度与时间的关系
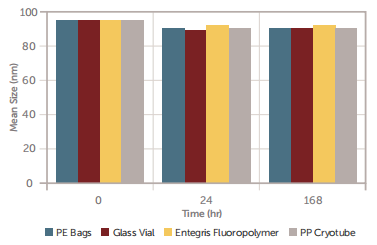
图3 mRNA LNP平均粒径与时间的关系
如图1至图3所示,在室温下储存168小时后,在工业标准的玻璃瓶、PP冷冻管、PE袋容器中存放的mRNA包封的LNP模型保持了几乎相同的脂质纳米颗粒浓度、mRNA浓度、包封效率和平均粒径,这表明 Aramus氟聚合物袋适用于医药用途。
然后将含有LNP悬浮液的冻存袋运送至加利福尼亚州 Entegris Goleta 工厂,使用Nicomp®DLS 和AccuSizer SPOS系统进行粒度的测试。Nicomp系统数据显示LNP尺寸从96nm增加到134nm,这很可能是由于随着时间的增加而发生的团聚。然后在AccuSizer SIS颗粒计数器测试袋子的颗粒数,检测0.5‒400µm范围的颗粒粒度。图4所示的结果绘制了T0和168小时后, Aramus含氟聚合物袋与聚乙烯(PE)袋的颗粒数/mL及其颗粒分布。

图4 不同一次性外壳中每毫升的颗粒浓度
图4中的结果表明在T0和168小时后PE袋中的大颗粒明显增多,这表明LNP可能存在大量团聚的现象,但是这些颗粒是不是PE袋中存在的污染物,由于SPOS无法分析其化学性质故无法确认。但是这里展现的颗粒浓度分布与内在蛋白聚集的展现较为一致6。
在审查这些结果时,Entegris决定调查Aramus冻存袋组件与其他SU冻存袋组件亚微米颗粒污染物含量。为了达到颗粒污染的Z高洁净度的检测能力,包括测量到10和25µm以下的尺寸。
冻存袋洁净度比较试验
购买了几种市售的SUS袋,并进行了颗粒污染比较研究。
步骤:
⚫ 测试Milli-Q超纯水以建立背景基线
⚫ 用上述Milli-Q超纯水以SA/V=6 cm2/mL的表面积与体积比填充250 mL冻存袋组件(遵循BPOG指导)
⚫ 在轨道振荡器上以40 RPM搅拌冻存袋2分钟
⚫ 将水从冻存袋转移到干净的烧杯中
⚫ 对烧杯中的水进行液体颗粒计数测试
AccuSizer SPOS系统设置:
传感器模式:summation
样品体积:5 mL
重复次数:4
流速:30 mL/min
图5显示了Aramus袋与品牌A的一种EVA袋的比较。

图5. 颗粒浓度/mL,Aramus袋与EVA袋
这些结果表明,Aramus聚酰胺含氟聚合物袋中的颗粒污染水平低于EVA材料袋。审查完这些数据后,在马萨诸塞州比勒里卡Entegris工厂继续进行额外的测试,将Aramus含氟聚合物与两种EVA型袋进行比较。在马萨诸塞州比勒里卡的研究中使用了与上述相同的设置和方案。
如图6所示,将两种类型的250 mL EVA冻存袋组件与250 mL Aramus冻存袋组件进行洁净度比较。Aramus组件始终符合USP<788>标准,而两种EVA袋有时超过USP<788>规定的限值。
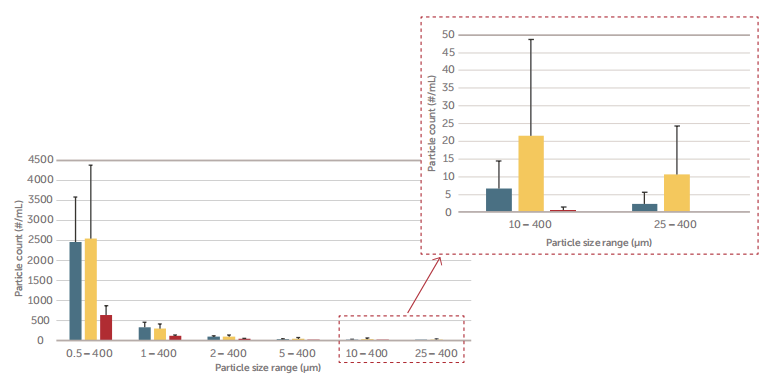
图6 Entegris(红色)、B品牌(蓝色)、C品牌(黄色)每毫升颗粒浓度(#/mL)与粒度(µm)。
图7 所示的结果还表明,与品牌B和品牌C的EVA冻存袋相比,Aramus冻存袋组件在>0.5µm范围内的颗粒污染水平低,约为B品牌的一半和C品牌的三分之一。
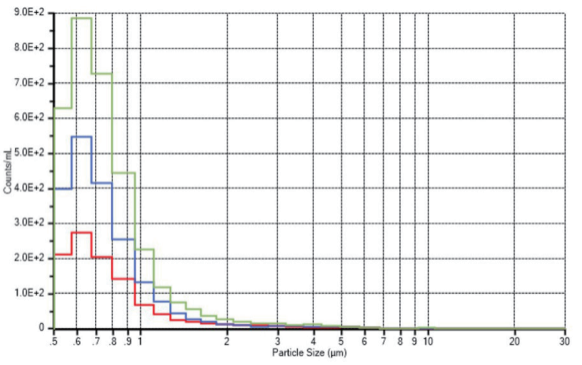
图7. Entegris(红色)、B品牌(蓝色)、C品牌(黄色)每毫升颗粒浓度(#/mL)与粒度(µm)。
结论
这项研究表明,Aramus含氟聚合物袋组件比竞争对手的袋清洁得多。Aramus冻存袋组件始终符合USP<788>标准,而竞争对手的冻存袋有时不符合标准。Aramus冻存袋组件能提供更一致的性能,为客户提供质量保证。我们还观察到,与竞争对手的EVA冻存袋相比,Aramus冻存袋组件在亚微米颗粒范围内的洁净度是其两到三倍,这表明Aramus冻存袋组件是用于生物制药行业应用的一个很好的一次性使用系统。
参考文献
[1] Recommendations for Testing, Evaluation, and Control of Particulates from Single-Use Process Equipment, BPSA 2014 report
[2] USP <788>, Particulate Matter in Injections
[3] Entegris Application Note, Aramus Single-Use Bag Particle Testing, November 2018
[4] Entegris Application Note, Monitoring Particulate Contamination in Medical Devices, March 2021
[5] Precision Nanosystems, Inc.,
[6] Chou, K. and Bumiller, M., Opportunities and Pitfalls in the Analysis of Subvisible Particles during Biologics Product Development and Quality Control, American Pharmaceutical Review, August 2020

上海奥法美嘉生物科技有限公司
仪器网(yiqi.com)--仪器行业网络宣传传媒