成功的内毒素检测自动化将如何积极地影响您的工厂?
2022-08-18413成功实施一个内毒素检测自动化项目不仅能会使QC 实验室检测更多的样品。在大多数公司中,业务的多个领域都可从精心设计的自动化技术中获益。
让我们考虑一下制药生产车间中因引入新技术而受获益的某些领域:
供应链和存储:当在存储方面对试剂和耗材进行Z 小化或简化时(例如,从低温到室温存储条件的过渡),这对仓储是有利的。记住系统使用的所有产品和耗材,并确保解决供应链安全和存储问题十分重要。对于内毒素检测,包括鲎试剂在内的生物检测的多种成份都需要低温存储,但是,新一代的自动化检测仪能显著减少鲎试剂的低温存储需求,并取消内毒素参考标准品(RSE)/ 内毒素对照标准品(CSE)的低温存储需求,因为内毒素标准品已经预嵌入在微孔板上,能在室温下存储并保持稳定。
验证和计量:使用可以在几天内完成验证的新一代技术,极大改善了系统实施和cGMP放行工作。仔细检查验证过程并确保可以使用新检测仪及时验证非常重要。此外,还应根据可以验证的Z 终产品数量以及检测仪维护的复杂程度来加以考虑。有关内毒素检测仪验证的更多内容,请参见第 7章。
质控 QC 实验室:任何内毒素检测项目的工作中 枢均是 QC 实验室。这里有使用检测仪的实际经验,以及增加检测通量、减少化验设置时间和提高其他运行指标(如重复检测率等)的机会。采用新技术需要考虑的问题包括QC 分析员培训、手动操作时间、软件管理和分析方法可比性研究。能更简单、更快速执行日常QC 检测的技术,但无需困难的培训或方法转移过程,是Z 有益的。软件也在 QC实验室的可用性、采用率和速度方面发挥重要作用。
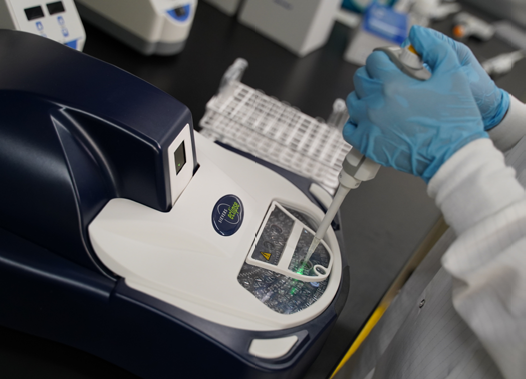
QA 与监管:当要求确保产品满足质量标准(包括内部标准、行业和安全标准)并符合政府监管法规时,制药生产的QA 和监管专业人员致力于以Z 高效的方式向患者提供安全、高质量的药品。但是,为了不牺牲质量,有时候速度和效率会受到影响。当评估新技术时,在数据可靠性、合规性、安全性和承受审计压力的能力等类别中有明确的“ 必须要求 ”。一旦满足这些标准,可通过简单快速的数据审核、签发和批次放行程序来实现额外的价值。
IT 和 IS:企业级软件解决方案使灵活性Z 大且仍能确保合规性,为当今的数据安全和可扩展性需求提供所需的能力。IT和IS团队通过使用能够定制化权限、易于进行数据安全保护、访问和管理,并可通过单个软件程序实现简单集成的技术,来支持药品生产、检测和市场销售放行工作。必须完全满足数据可靠性和 21CFR 第 11部分的要求。
简化内毒素检测——从库存到批次放行
Sievers Eclipse*月食细菌内毒素检测仪
Sievers Eclipse月食细菌内毒索检测仪使用微流控自动化和Z 新的兼容软件来简化您内毒素检测程序的每步,从供应链和存储 到验证、常规检测和签字放行。
通过以下方式降低成本并Z 大程度减少仓储:
■ 微孔板仅需在室温条件下进行储藏
■ 鲎试剂冷藏可降低10倍
■ 无需存储RSE或CSE-内毒素标准品已预先存储于Eclipse微孔板中
使用以下方式改进系统实施和cGMP放行:
几天内即可完成系统验证
每个Ecllpse微孔板能够验证7种Z 终产品
Z 少化台式分析仪的维护量-无需机器人
通过以下方式简化并提高检测量:
■ 9分钟内即可轻松完成检测,少于30个移液步骤
■ 自动执行标准曲线、阳性产品对照PPC和自动混合
■ 仅需要简短的分析人员培训
■ 出现错误的机会有限
■ 省时的模板和附件信息库
通过以下方式简化产品放行:
■简化批实检测、数据审样和放行
■远程数据审核和样品签核
■全面的专属性检测的审计遍踪
通过以下方式Z 大化灵活性并确保合规性:
■ 企业级的软件解决方案
■ 自定义权限
■ 数据可靠性和ALCOA+
■ 21 CFR Part 11
-
- Sievers Eclipse月食细菌内毒素检测仪
- 品牌:Sievers/威立雅
- 型号:Eclipse月食


