DVS钙钛矿吸湿稳定性
2023-07-21507杂化钙钛矿甲基铵碘化铅(MAPI)的水化形成与损失
采用水蒸汽吸附和解吸法研究了杂化钙钛矿甲基铵碘化铅(MAPI)的水化状态。精确的水蒸汽吸附等温线将在开发和保护MAPI器件免受湿气损伤方面发挥重要作用。
引言
杂化钙钛矿甲基铵碘化铅(CH3NH3PbI3)由于其潜在的太阳能转化为直流电的应用装置而引起越来越多的关注。然而,真正的挑战在于开发在不同环境条件下工作的器件,因为MAPI可能形成一水合物(CH3NH3PbI3·H2O)或二水合物((CH3NH3)4PbI6·2H2O)晶体相,MAPI器件的电荷输运特性取决于这些相中的甲基铵离子和水分子网络[1]。MAPI晶体在低于40℃的水溶液中形成无色的单水合甲基铵碘化铅(CH3NH3PbI3·H2O)。当MAPI 在Pb(NO3)2和碘化铵溶液的母液中冷却到40℃以下时,会产生淡黄色的二水晶体。湿度的存在已被证明会显著影响形态,并被声称会导致太阳能电池性能的改善。然而,水的存在也被认为可以催化MAPI的不可逆分解 变成水的HI,固体的PbI2和CH3NH2,或作为气体释放或溶解在水中[2]。因此,MAPI太阳能电池暴露在相对湿度大于50%的环境中会对器件性能产生迅速的不利影响。本文描述了动态蒸汽吸附可以用来检测和表征这些水合相作为环境相对湿度的函数。
方法
动态蒸汽吸附(DVS)是一种行之有效的蒸汽吸附等温线测定方法。用于这些研究的DVS仪器使用质量分辨率为±0.1μg的SMS超天平以重力方式测量蒸汽的吸收和损失。高质量分辨率和优良的基线稳定性使仪器能够测量极少量探针分子的吸附和解吸。样品周围的蒸汽分压通过使用电子质量流量控制器混合饱和和干燥载气流来控制。通过将整个系统封闭在恒温箱中,温度保持恒定±0.1°C。
MAPI由伦敦帝国理工学院Piers等[1]使用参考文献[3]中描述的程序制备。在DVS实验中,将39mg 样品放在样品盘中,在25°C下以0%RH干燥5小 时,以去除任何残留的水分,然后暴露在一系列阶梯相对湿度(±0.5%)中。当样品质量变化率低于~0.002% /min或~ 3 h时,实验进入下一个RH阶段。在解吸过程中,湿度增加到95%RH,然后以类似的方式降低。实验在50°C重复进行。
结果
MAPI样品在25℃,0 ~ 95% RH范围内的吸湿动力学如图1所示。红线表示质量变化百分比(基于干值)随时间的变化,而蓝线表示相对湿度随时间的变化。对应的等温线如图2所示,其中红线沿吸附分支,蓝色轨迹沿解吸分支。
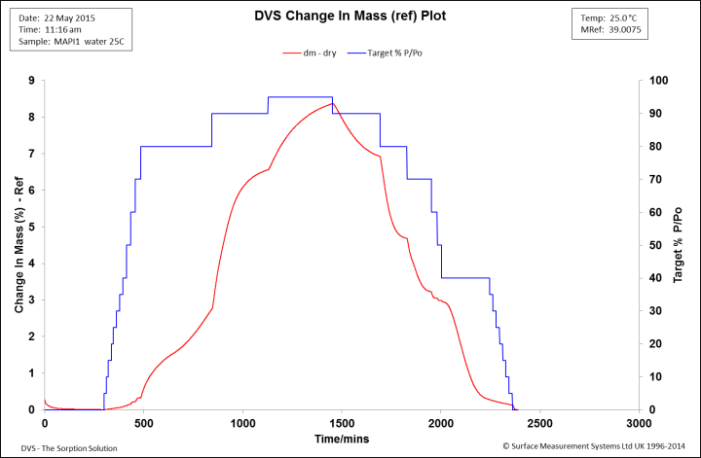
图1. MAPI二水合物样品在25℃时的吸水动力学
在初始干燥阶段,质量损失不显著,表明起始物料为无水形式。MAPI一水合物的分子量为637.9 amu,损失一个水分子将损失3%的重量(基于干值619.9 amu)。考虑到在初始干燥阶段没有质量损失,DVS数据表明起始样品不处于水化状态。从图1可以看出,当相对湿度增加到70%以上时,吸湿率显著增加,在95% RH时达到~8.3%。在解吸阶段,样品质量在70% RH阶段下降到原始质量的3.2%。在70% ~ 50%RH之间,质量几乎没有变化,然后在RH = 0%时,质量下降到~ 0.2%,然后下降到0.0%,表明这是一个可逆过程。
根据下面的化学方程,我们可以计算出从MAPI到一水化合物的转变应该导致样品质量增加3%。
4CH3NH3PbI3+4H2O ⇌4[CH3NH3PbI3H2O]
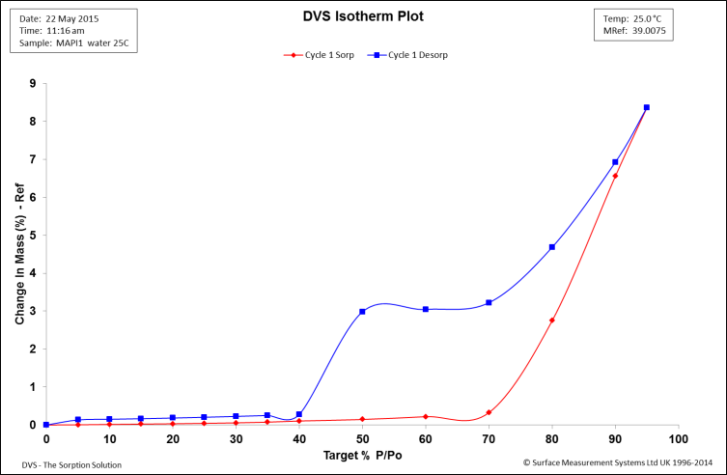
图 2. 25°C,MAPI二水合物水吸附 (红)和脱附(蓝)等温线
图2中的等温线显示在50 RH和70% RH之间有一个宽的迟滞间隙。这通常表明水合物的形成,样品在低RH时失去水分子,而不是获得水分子。根据吸收量,我们可以估计水化组分的化学计量学。在50% RH的解吸步骤中,样品在水中保留约3%的干重。利用公式1,我们可以估计这种水化物种的化学计量学:
由式1可知,在解吸50%RH阶段,水化组化学计量为1.0,表明为一水组分。在相为50%或60%时,吸附与解吸等温线的吸值可取3.0%,对应于不含表面吸附贡献的吸收率。
在60%-80%RH范围内,MAPI样品暴露于水蒸汽时,会占用相对大量的水,从而转变为一水合相。在解吸阶段,样品保持一水合化学计量直到低于50%RH,再次失去一个水分子。
从图1中可以看出,样品在80%-90% RH阶段的吸水量相对较大,此时质量急剧增加。质量吸收在90%RH步骤结束时完成,因为质量已接近平衡,样品质量进一步增加3.5%,这对应于二水物种的形成。然而,在90%和95%RH时,样品质量没有达到平衡,任何水合物的形成都不会完全。在解吸阶段,当湿度从90%RH降低到70%RH时,样品质量下降3.2%,表明样品回到了一水形态。
DVS实验结果与理论值之间的相关性,以及Leguy等人[2]对MAPI晶体暴露在70% RH下的XRD表明,一水相在70%-50%RH之间保持稳定。然而水化状态的变化在动力学上是有限的,长时间暴露在高%RH值下可能会导致二水合物的形成。
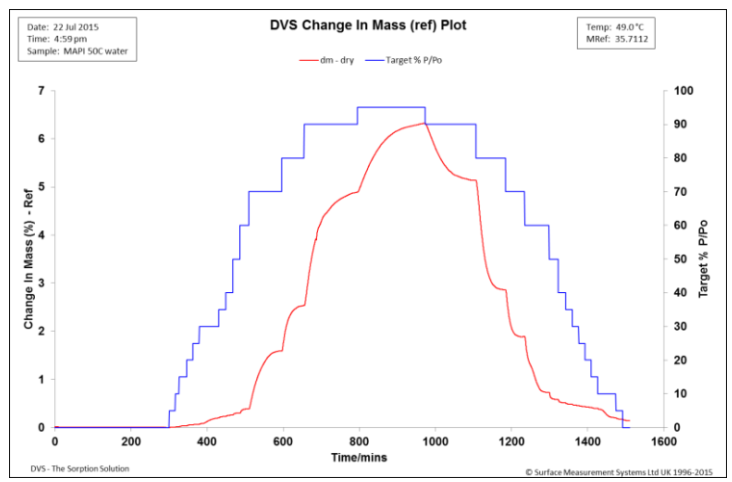
图3. 50℃,MAPI二水合物水吸附动力学
实验温度为50℃,考察了温度对水合物种类的影响。从图3中可以看出样品质量在25%RH左右时增加。然后在60%RH以上,每个湿度吸湿量都增加。然而与25℃时相应的%RH值相比,吸湿量相对较小。这是由于在更高的温度下,分子的流动性更大,这也会导致更快的动力学。
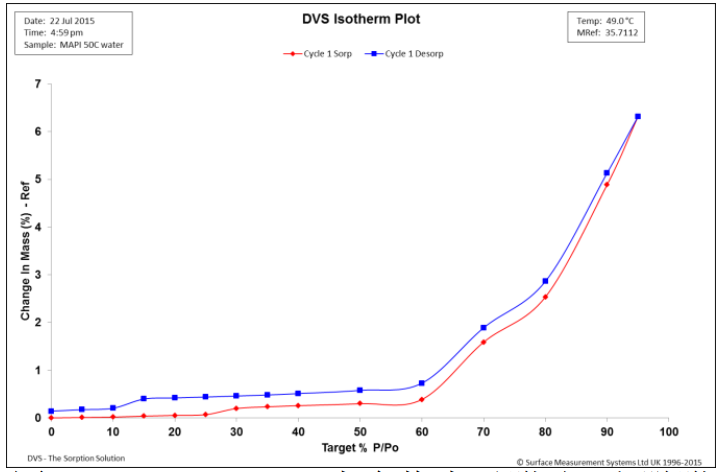
图4. 50℃,MAPI二水合物水吸附(红)和脱附(蓝)等温线
图4显示了整个%RH范围内的迟滞回线,在0%RH时仍保持“open”状态。相对于25°C的实验(图2),更小的滞后间隙证实了水化态的形成是可逆的,在50°C时动力学限制显著减少。
结论
研究了杂化钙钛矿甲基铵碘化铅(MAPI)水合物的形成和损失。水化物种的化学计量学是由两种温度下相对湿度的相应重量增加决定的。实验表明在室温下,向水化形态的可逆转变在动力学上受到限制,从而导致材料吸水和脱水的滞后。在较高的温度下,这种转变发生时没有滞后现象,而且动力学更快。先前的研究和二水化合物的直接合成及其随后的干燥也表明恢复了原来的单水化合物和MAPI结构,证实了DVS的结果在这些反应的可逆性方面。
参考文献
Barnes, P. R. F. et al.The hydration of organic-inorganic hybrid perovskites: theory and experiment. In press.
Leguy, A. et al. The reversible hydration of CH3NH3PbI3 in films, single crystals and solar cells. Chem. Mater. 150405140636003 (2015).
[3] Im, J.-H., Lee, C.-R., Lee, J.-W., Park, S.-W. & Park, N.-G. 6.5% Efficient Perovskite Quantum-Dot-Sensitized Solar Cell. Nanoscale 3, 4088 (2011).

