可调刚性PLGA壳-脂质核纳米颗粒在2D和3D肺癌细胞模型中增强肺siRNA递送
2024-02-1958面对世界范围内的肺癌相关死亡的威胁,小干扰RNA(siRNA)可以沉默肿瘤相关信使RNA(mRNA),以增强抗肿瘤效果,解决耐药问题。然而,如何通过增强基因沉默来增加肺肿瘤靶向性和穿透性是需要解决的问题。因此,本研究的目标是探讨设计非病毒siRNA载体以增强吸入肺肿瘤治疗的可行性。在这里,通过在载有siRNA的阳离子脂质体(Lipoplexes)上涂覆PLGA,通过微流控技术制备了壳核基聚合物-脂质杂化纳米颗粒(HNPs)。透射电子显微镜和能量色散谱研究表明,HNP由PLGA壳和脂质核组成。原子力显微镜研究表明,通过改变PLGA壳的厚度可以很好地调节HNP的刚性。设计的HNPs具有黏性惰性,在黏液和BALF中稳定性增加,安全性良好,增强了黏液穿透性和细胞摄取。关键的是,具有最薄的PLGA壳的HNP1在A549细胞中表现出优异的转染效率(84.83%),与脂质体和Lipofectamine 2000相当,其在A549-3T3肿瘤球体中的肿瘤渗透性是脂质体的1.88倍。HNPs内化后,不仅观察到内吞逃逸,还观察到溶酶体外泌。在A549-3T3肿瘤球体中,HNP1的转染效率(39.33%)是脂质体的2.26倍。此外,HNPs在通过软雾吸入器雾化时表现出良好的稳定性。总之,我们的研究揭示了HNP1在通过吸入传递siRNA治疗肺癌方面的巨大潜力。
肺癌是世界上最常见的恶性肿瘤之一。非小细胞肺癌(NSCLC)约占所有肺癌的80-85%,约80%的患者在诊断时已经处于晚期(III或IV期)。虽然晚期NSCLC患者的化疗和放疗已经相对规范,而精准医学的发展促进了小分子抑制剂在靶向治疗中的应用,但过去40年的预后仍然较差,5年生存率非常低(∼16%)。肿瘤具有不同的突变水平,而传统治疗往往忽视了肿瘤的特异性。此外,肿瘤的获得性和固有耐药性是现有治疗的主要挑战,因此迫切需要开发新的治疗方法来解决这些问题。
随着COVID-19的爆发,基因治疗受到了极大的关注。RNA(核糖核酸)治疗具有高特异性和广泛靶点的优势。目前,NSCLC患者中已经鉴定出多个靶点,包括表皮生长因子受体(EGFR)、血管内皮生长因子(VEGF)和Kirsten大鼠肉瘤病毒癌基因同源物(KRAS)等。基因抑制治疗可应用于上述靶点。小干扰RNA(siRNA)(约13 kDa)通常是一种长度为21至23个碱基对(bp)的双链RNA。根据靶点的特性,可以设计siRNA的序列,以实现高度特异性的靶向治疗。当siRNA被输送到肺癌细胞的细胞质中时,它可以对肿瘤相关信使RNA(mRNA)产生基因沉默,从而抑制癌细胞增殖,防止肿瘤转移,并诱导癌细胞凋亡。
然而,尽管siRNA在肺癌治疗中具有很大的潜力,但它不稳定,容易被RNA酶降解。因此,开发安全有效的载体来保护裸siRNA是绝对必要的。对于肺癌治疗而言,肺给药是一种优越的途径,它可以实现药物的高局部浓度,同时减少药物剂量和全身暴露,从而降低毒性。然而,除了增加局部沉积外,可吸入颗粒必须能够穿透黏液层,防止被纤毛清除,并避免被巨噬细胞吞噬。除了细胞外屏障外,还需要克服细胞内屏障,在肿瘤穿透后有效地逃脱内/溶酶体。因此,一个理想的肺癌治疗siRNA给药系统应该满足以下要求:(1) siRNA被有效地封装在载体中; (2)可吸入载体需要克服肺给药的挑战; (3)载体必须穿透到更深的肿瘤; (4) siRNA必须在降解前逃脱内/溶酶体。
在广泛报道的基因给药系统中,与病毒载体相比,非病毒载体的免疫原性低,易于设计和合成。特别是阳离子脂质体(CL)具有体外转染效率高、载药量大、结构灵活、易于大规模生产等优点。然而,CL的高表面电荷导致严重的细胞毒性,并且它还与肺细胞的负电荷表面存在潜在的不良相互作用。此外,CL在肺微环境中不稳定,黏液渗透性差,这使得CL不利于肺部递送。此外,CL的肿瘤渗透性差使其不适合肺癌的治疗。基于上述问题,我们的假设是,通过应用CL来有效地压缩和保护siRNA,同时使用负电荷和可生物降解的聚(D,L-乳酸-co-乙醇酸)(PLGA)作为涂层材料来覆盖CL的高正表面电荷,不仅提高了CL的安全性和稳定性,而且在肺部递送后可以实现根据黏液和肿瘤渗透性所需的可调刚度。
因此,本文的目标是开发安全有效的非病毒载体,适用于通过肺部siRNA递送进行肺癌治疗。首先,利用微流控技术制备空白CL,然后通过两步法获得siRNA载体CL,接着利用微流控技术的高混合和溶剂扩散获得聚合物-脂质杂化纳米颗粒(HNPs),然后利用多种技术(表面电位测量、透射电子显微镜和能谱)来阐明HNPs的壳核结构,并通过原子力显微镜研究PLGA对总脂质重量比对HNPs刚性的影响。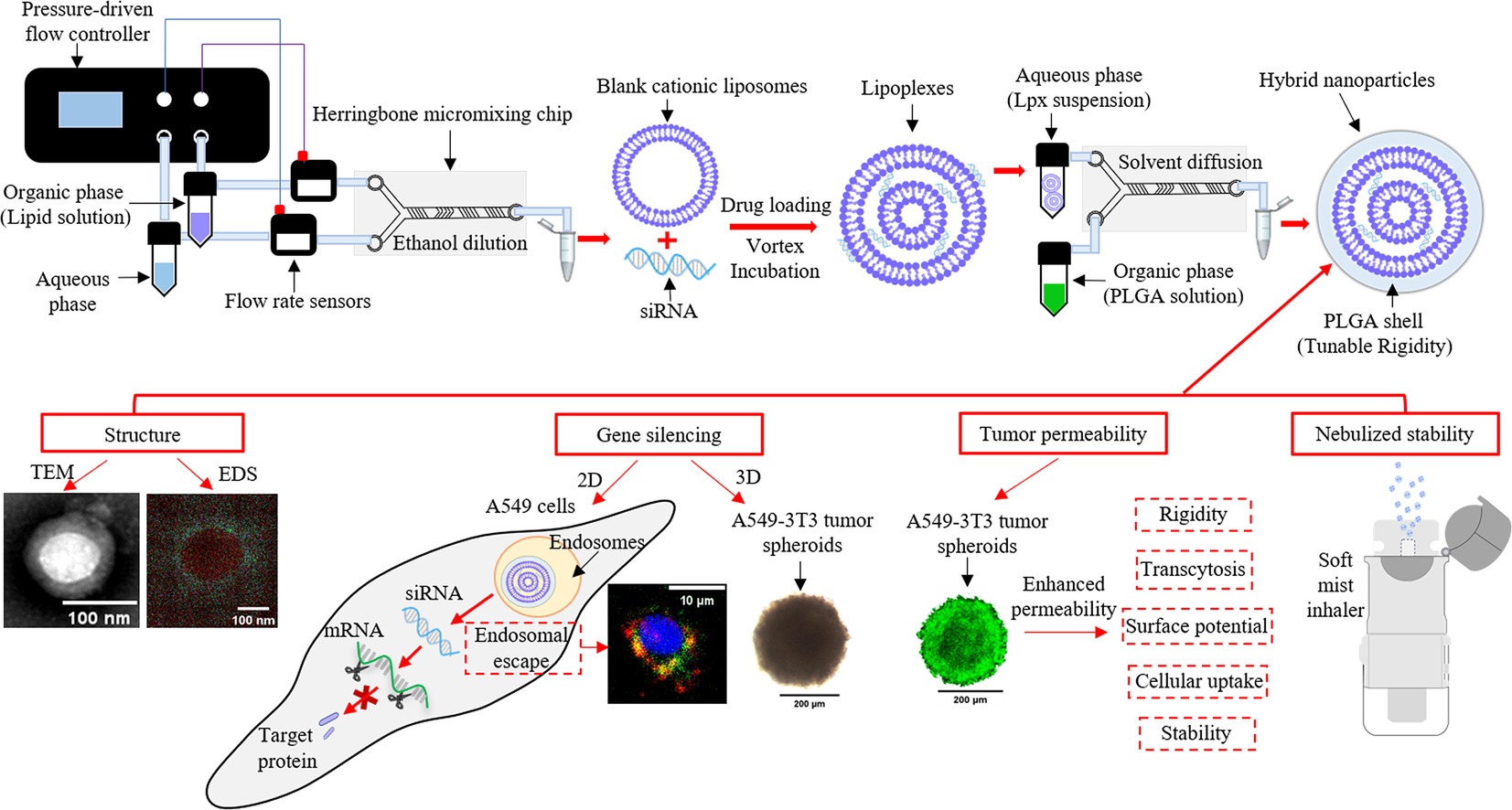
参考文献:
Wang H, Yuan Y, Qin L, Yue M, Xue J, Cui Z, Zhan X, Gai J, Zhang X, Guan J, Mao S. Tunable rigidity of PLGA shell-lipid core nanoparticles for enhanced pulmonary siRNA delivery in 2D and 3D lung cancer cell models. J Control Release. 2024 Jan 19;366:746-760. doi: 10.1016/j.jconrel.2024.01.029. Epub ahead of print. PMID: 38237688.

