在今日《科学》的论文中,André Nussenzweig研究团队以有丝***后的神经元和巨噬细胞为研究体系,发现DNA主动去甲基化对于增强子激活是必要的,并且解释了神经元和巨噬细胞增强子上DNA单链损伤的来源以及阐述其中的机制。

据研究者介绍,在哺乳动物细胞中,5-甲基胞嘧啶(5mC)是***主要的DNA修饰,它对于发育和细胞分化有重要作用。5mC可被TET酶氧化为5-羟甲基胞嘧啶(5hmC)、5-甲酰基胞嘧啶(5fC)和5-羧基胞嘧啶(5caC),引起DNA去甲基化。
在DNA主动去甲基化过程中,5fC和5caC被胸腺嘧啶DNA糖基化酶(TDG)切除产生无碱基位点,并后续产生DNA单链损伤。其能通过碱基切除修复(BER)途径***终修复转化为C碱基。
根据过往研究数据,研究者推测单链DNA损伤可能与TET-TDG介导的5fC/5caC切除有关。利用细胞工程获得的兴奋性神经元(iNeuron),研究者降低了细胞TDG水平,结果发现此行为可让神经元中可以积累大量的5fC/caC。
随后,研究者利用课题组开发的DNA单链损伤检测技术发现,降低TDG水平几乎消除了DNA单链损伤。这也说明,神经元中DNA单链损伤来源于TDG依赖的DNA主动去甲基化。
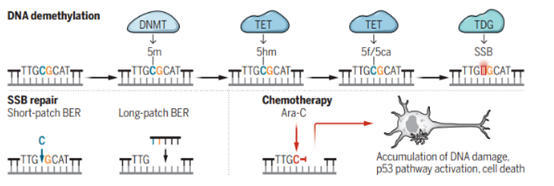
▲研究示意图(图片来源:Active DNA demethylation damages DNA,DOI:
除了在神经细胞增强子上观察到重复出现的DNA损伤修复事件,研究者还使用了由前体B细胞转分化来源的巨噬细胞作为测试对象。通过CRISPR/Cas9敲除TET2和TDG蛋白,研究者也在巨噬细胞中发现了主动去甲基化引起的DNA单链损伤和修复过程。
不过两者也有着略微的区别,巨噬细胞偏好使用短补丁碱基切除修复(short-patch BER)以填补单核苷酸断裂缺口,而神经元会同时使用长补丁碱基切除修复 (long-patch BER)和短补丁碱基切除修复。
根据论文,TDG缺失不会影响巨噬细胞和神经细胞的分化,却会在分化过程中让数千种基因的表达发生变化。这对细胞的行为是有影响的,例如TDG缺失削弱了巨噬细胞吞噬细菌的能力。而TDG被敲除,会部分影响神经元分化成熟相关基因的表达上调,包括神经突触前信号通路调控的相关基因。
研究者指出,新研究发现的机制对于肿瘤治有一定启示意义。在DNA 主动去甲基化过程中,若使用抗肿瘤胞嘧啶类似物(Ara-C)中断DNA修复会触发 TDG 依赖性DNA损伤应答和神经元死亡,这表明神经元在正常分化和分化成熟后内在的生理活动可能会导致化疗造成的神经损伤。
André Nussenzweig课题组博士后王东鹏,吴薇(兼共同通讯作者,现为中科院分子细胞科学***创新中心研究员)和研究科学家Elsa Callen为该论文的共同***作者。
现阶段核酸检测是分析疾病的重要手段,洛阳吉恩特生物giant-bio自主研发生产的纳米核酸提取磁珠(DNA/RNA提取磁珠) 磁响应时间迅速,提取效率高,可明显缩短实验时间,提高实验效率,并在提取结果上保持稳定,另外羧基磁珠和氨基磁珠也是制作免疫磁珠的重要原料。

 评论
评论