发表于《自然》杂志的***新研究中,一支来自中国的研究团队取得了重要突破。他们将人的多能性干细胞转化为8细胞阶段的全能性胚胎样细胞(称作“8C样细胞”),后者能发生合子基因组激活、保留了发育成所有组织与器官的潜力。这项突破为器官再生与合成生物学的新进展奠定了重要基础。

在此之前,已经有研究能够将多能性干细胞转化为囊胚的内细胞团状细胞。而***新研究更进一步,希望将多能性干细胞转化成人类发育更早阶段的全能性细胞。
人类受精卵形成之后,基因组***初会保持沉默状态。当受精卵***到8细胞阶段时,合子基因组才会迅速激活。因此,研究这一阶段对于理解生命发育至关重要。
为了将人的多能性干细胞转化为8C样细胞,研究团队开发出一种化学“鸡尾酒”:从一系列靶向信号或表观遗传通路的抑制剂中,筛选出能完成转化的试剂组合。在这一过程中,研究团队还借助了单细胞基因组测序:将细胞注射进小鼠体内,经过进一步发育后,通过测序识别并分离出8C样细胞。
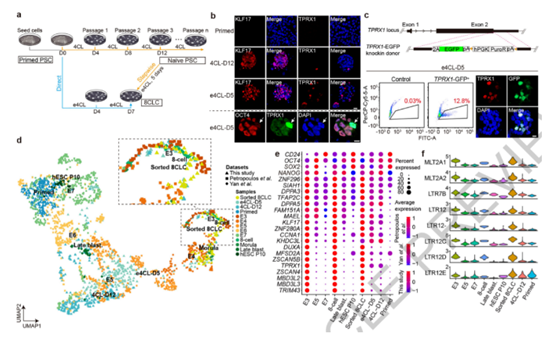
▲研究团队将人的多能性干细胞转化为8C样细胞
由此,研究团队通过一种无需转基因、快速、可控的方式,成功利用人的多能性干细胞生成8C样细胞,后者在转录和表观遗传上均与真正的8细胞期胚胎相似。在这个转化过程中,DPPA3和TPRX1基因起到关键作用:前者导致了DNA脱甲基化,而后者是8C样细胞基因网络的关键调控因素。
作为发育早期的全能干细胞,这些细胞应该有潜力分化出所有的胚胎细胞类型,进而产生发育必需的组织和器官。随后的实验证明了这些细胞的全能性。在体外与体内实验中,8C样细胞均能产生胚胎和胚胎外的细胞系:其中,体外实验产生了滋养层干细胞和类囊胚,生物活体实验生成了畸胎瘤。
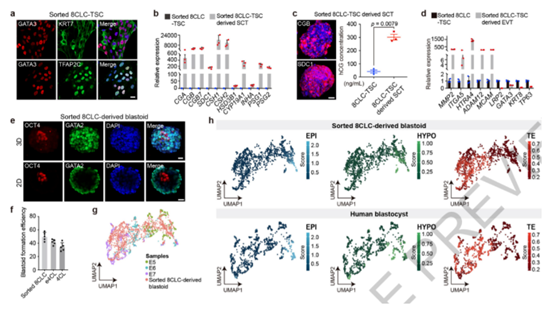
▲8C样细胞在体外生成了滋养层干细胞和类囊胚
这项研究***证明了转化后的细胞能在活体内产生胎盘组织。毫无疑问,这项研究将帮助拓展对人类早期胚胎发育的理解,也为一系列后续应用铺平了道路。未来,这些细胞不仅有望用于再生医学,实现人类器官的再生、减少对器官捐献的依赖,还能用于生成人造囊胚与类囊胚。这种研究手段还能帮助科学家研究人类胚胎发育、治疗早期发育相关的疾病。
“全能性8C样细胞经过3次***,就能产生胚胎状态的受精卵。相比于多能性干细胞,这些细胞不仅能分化成胎盘组织,还有潜力发育成更成熟的器官,为正在等待器官移植的患者带来福音。”来自中科院广州生物医药与健康研究院的科学家们表示。
生物磁珠对细胞筛选的方法已日渐成熟,原理是将包被一抗的磁珠与细胞表面对应的分子特异性结合,或者将包被二抗的磁珠与已经与细胞表面分子特异性结合的一抗结合。磁珠携带与之结合的细胞吸附与分离柱或试管上,实现阳性细胞或阴性细胞的分离。洛阳吉恩特生物自主研发生产了各类生物磁珠,可以实现稳定的实验结果。

 评论
评论