
发表期刊:Water research.2020.
影响因子:7.913
作者单位:1 Office of Research and Development, U.S. Environmental Protection Agency, 26 W. Martin Luther King Dr., Cincinnati, OH, 45268, USA. Electronic address: jahne.michael@epa.gov.
2 Office of Research and Development, U.S. Environmental Protection Agency, 26 W. Martin Luther King Dr., Cincinnati, OH, 45268, USA.
基于风险的现场分散废水再利用处理需要有关源水体中病原体的发生情况和密度信息;废水分散再利用系统处理指南制定的一个基本障碍是,缺乏现场或本地收集的废水病原体特征数据,包括灰水(来自浴室的水槽、浴缸/淋浴和洗衣机的水)、黑水(厕所和厨房水槽的水)以及混合废水(混合的灰水和黑水)。传统的荧光定量PCR(qPCR)检测灰水中病原体的灵敏度不够,病原体密度可能接近检测灵敏度极限。以流行病学为基础的病原体建模作为一种替代方法已被提出,然而,鉴于缺乏现场收集的废水病原体定量数据,这些病原体模拟结果没有在实际环境的病原体研究数据中得到验证。
为了改进以往废水中低病原体密度的检测方法,本研究采用微滴式数字聚合酶链式反应(ddPCR)方法,对来自三个不同建筑规模分散收集系统的未经处理的灰水(n=50个样本)和混合废水(即包括黑水,n = 28)中的病毒性肠道病原体(诺如病毒基因组GI、GII和人类腺病毒)进行定量分析。然后,用这些ddPCR定量结果与用于模拟非饮用现场废水再利用的基于流行病学的病原体模型和qPCR的结果进行对比。
这项研究表明,ddPCR可在废水和灰水中定量病毒,ddPCR的高灵敏度相对qPCR允许更大的定量检测率,ddPCR检测的浓度与先前报道的基于流行病学一定规模人群中病原体感染发生的建模结果基本一致,ddPCR定量结果支持针对现场非饮用水重复使用已发布的病原体减少目标。
通过双重ddPCR反应对样本中的腺病毒(用FAM标记)和内部扩增子对照(IAC:由一个线性化的定制基因组成,标记为VIC) 进行定量,使用双重RT-ddPCR反应定量诺如病毒(用FAM标记)和第二个对照IAC (标记为VIC)。对所研究的三个分散废水和灰水收集系统,使用ddPCR可定量病毒性肠道病原体(图1),有27/28个混合废水样本和3/50个灰水样本可量化诺瓦克病毒GII浓度;腺病毒可量化的样本比例是7/50个灰水样本和4/28个混合废水样本;在11/28个混合废水样本中,诺如病毒GI是可量化的;在灰水中无法定量到诺如病毒GI (0/50个样本)。在ddPCR可量化的样本中,混合废水的腺病毒、诺如病毒GI和诺如病毒GII浓度分别为2.2 ~ 3.2、2.1 ~ 4.0和5.2 ~ 7.9 log10基因组拷贝/L;灰水的腺病毒和诺如病毒GII浓度分别为2.0-3.8和2.1-2.5 log10基因组拷贝数/L。每个靶标病原体可定量浓度的样品数量,ddPCR比qPCR多(图1),显示出ddPCR比qPCR灵敏度高。在混合废水中,诺如病毒GII的ddPCR定量率(96%)与可比较的1000人模拟结果(所有基因组的总和为99%)非常吻合(图1)。
图1 在三个分散式混合废水(WW1)和灰水(GW1和GW2) 收集系统中,腺病毒(AdV)、诺如病毒基因组I(NoVGI)和NoVGII通过ddPCR和qPCR可量化样本百分比。WW-Sim和GW-Sim列显示先前发表的这些病原体基于流行病学类似规模的模拟结果。
在混合废水中,诺如病毒GII的密度足够高,可以通过ddPCR和qPCR两种方法进行定量(图2),检测到的密度范围是5.2-7.9 log10基因组拷贝/ L,并且相关性良好(R2 = 0.96),表明了ddPCR方法在废水基质检测中的准确性。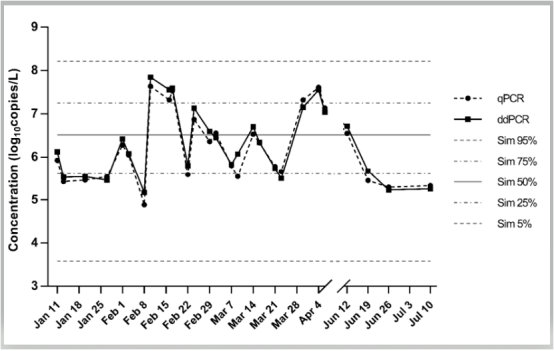
图2 通过ddPCR和qPCR测定分散混合废水中诺如病毒基因群II(诺如病毒GII)的浓度。结果与先前发表的基于流行病学的模型相比较,“Sim”线表示日模拟的各个百分比(n=365×10000)。
尽管数量有限的灰水样本可定量检测腺病毒(n = 7/50)和诺如病毒(n = 3/50),但ddPCR检测到的浓度(分别为2.0–3.8和2.1–2.5 log10基因组拷贝数/ L)都在先前发表的由100人和1000人规模模拟预测结果的范围内(图3)。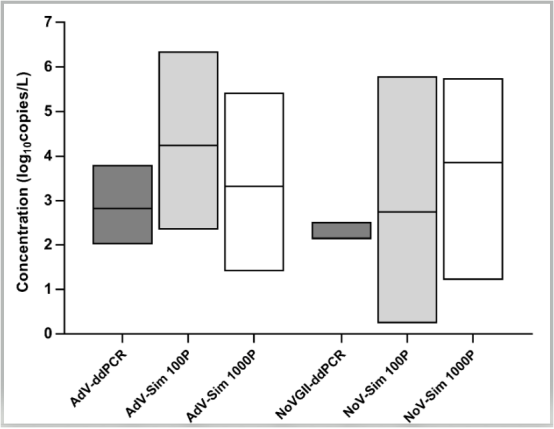
图3 使用ddPCR测定灰水的腺病毒(AdV)和诺如病毒基因组II (NoVGII)浓度和先前发表的基于流行病学的病原体模拟(100和1000人规模病原体模拟,分别是Sim 100P和Sim 1000P)。
本研究的ddPCR测定结果支持已公布的用于现场非饮用水重复使用的病原体的检测, ddPCR测定的以往无法检测到的病毒性肠道病原体浓度结果与先前模拟的浓度模型非常吻合。这项研究提供了新的ddPCR定量肠道病毒数据,以支持未来的研究工作。这是第一个关于灰水和现场收集的混合废水中诺如病毒浓度的定量报告。这项研究结果将有助于评估分散式供水系统的安全性和制定分散式废水再利用风险处理指南。
关于永诺

广州永诺生物科技有限公司成立于2010年,总部位于广州国际生物岛,是一家专注于医学科学技术开发与服务、分子诊断产品研发与生产的高新技术企业。公司目前占地面积近6000㎡,其中硕、博士以上学历员工占比近40%。公司依托先进的技术力量以及优秀的人才储备,在科研服务、医学检测和数字PCR产品三大业务上保持领先的竞争优势。
公司成立至今申请国家专利40多项,授权21项,计算机软件著作权8项,广东省高新技术产品证书8项,省、市等科技计划项目10多项,2018年入围了大湾区生物科技创新企业50强,获得国家高新技术企业,广州市科技创新小巨人企业、广东省高新技术企业培育库入库企业、广州市企业研发机构等荣誉称号。
永诺医疗是永诺生物的全资子公司,以“中国智造”为己任,专注于数字PCR仪器与应用试剂的研发,并于2017年成功研发了国内首发拥有完全自主知识产权的MicroDrop®系列微滴式数字PCR系统并投入生产。
 ZG疾病预防控制ZX病毒病预防控制所成功举办第六届病原体核酸检测新技术高级培
ZG疾病预防控制ZX病毒病预防控制所成功举办第六届病原体核酸检测新技术高级培
 你知道制药废水深度处理工艺技术分析吗?
你知道制药废水深度处理工艺技术分析吗?
 Gene-π数字PCR学堂: 在核酸定量中数字PCR方法学转换及应用(杭州站
Gene-π数字PCR学堂: 在核酸定量中数字PCR方法学转换及应用(杭州站
 为健康护航 | 监测废水中的新冠病毒
为健康护航 | 监测废水中的新冠病毒

 评论
评论