数据和记录在我们的生活工作中无处不在。在疫情爆发期间,是不是很多小伙伴都像小梅一样,下载某个程序或软件,提交自己的信息查看自己有无异常,是否属于密切接触者。这就是大数据!在这个特殊时期里,我们可以看到大数据、数字化信息为疫情控制提供了极大的便利!
对于制药行业来说,电子记录的方式被越来越多的制药企业所认可并采用。NMPA、FDA等监管机构,也在推动制药企业进行电子记录逐步取代纸质记录的改革。
各位老师有没有遇到过这些问题:目前法规的Z新动态是什么?以前能通过审计,现在却发现了新问题?继续使用纸质记录会有什么风险?流程或文档中发现来源不一致的时候,应该采取什么措施?
渴望知识的小伙伴们是不是都憋坏了?
这次Bob McDowall为我们准备了专门的议题:药企记录中的风险和错误管理,来帮助制药行业的小伙伴解惑。他是一位经验丰富的审计官,撰写了许多有关制药行业电子记录和数据完整性合规性文章,相信大家一定能满载而归!
主要议题
Part 1
•概述.
•灵活合规--制药行业法规理解及动态.
•现今的纸质记录的风险是什么?
•基于观察的USP方法的关键方面.
•空白纸质表单及其管理费用.
•与风险相比,您应该如何评估合规成本?
Part 2
•针对违规行为和调查结果的行动有哪些?
•非正式测试.
•在软件更新方面你有什么建议?
•报告问题的Z佳时间?
•合规成本.
•平台化解决方案 - 经济GX的计算机化系统验证(CSV).

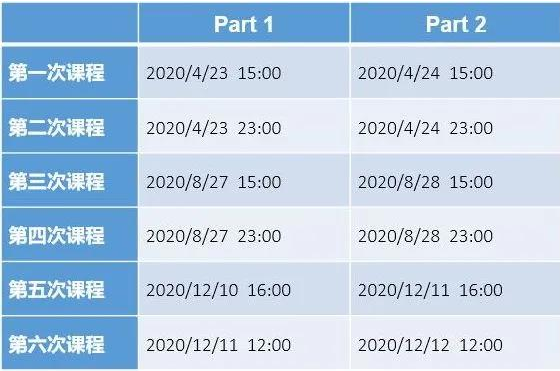
直播时间
整个在线讲座分两个部分,语言为英文,每部分时长均为 50 分钟,分别在多个时段进行,您可以选择自己方便的时间段收看。
参与方式
只需识别下方二维码,即可报名参加!
diyi部分

第二部分

除此之外,我们还为小伙伴们准备了更多的在线研讨会,对自动实现数据可靠性、精益实验室、21CFR Part 11的合规性感兴趣的,尤其是疑惑单机仪器电子记录是否合规问题的小伙伴们,可以识别下方二维码报名预约。

议题简述:
通过自动化实现数据可靠性 - 问题及解决方案.
如何避免“死于合规” - GX且成本可控的确保电子记录合规的计算机化系统验证.
仪器上的电子记录 - 符合21 CFR Part 11要求的单机仪器?
精益实验室原理及梅特勒-托利多的解决方案.

梅特勒-托利多实验室平台化软件LabX助您解决更多分析仪器的数据可靠性及电子数据的管理问题!

 评论
评论