2019年12月底武汉发现新型冠状病毒肺炎以来,感染确诊病例和疑似病例数量仍在不断上升,疑似病例的快速确诊迫在眉睫。目前临床上确诊新型冠状病毒肺炎病例,Z通用的方式仍然是在临床观察的基础上,采集痰液、咽拭子等呼吸道标本进行病毒核酸基因检测,并作出病原学诊断。目前核酸检测的准确性问题牵动了很多人的心,除去该病毒的一些特有特征外,检测过程中的每一个环节涉及的科学仪器和操作步骤都可能对结果产生影响。
目前新冠状病毒核酸检测主要通过PCR检测的方法,其对试验场地、检验仪器及操作人员的要求都非常高,轻微的污染就可能对结果造成偏差。另外,对检测样本保存条件和设备也有很严苛的要求。并且,由于新冠状病毒的传染危险性,防护准备和后续的消毒处理对整个检测实验来说也异常重要。Cole-Parmer作为一家专业的科研仪器、设备、耗材供应商,可以为新冠状病毒核酸检测提供从防护,采样,样本保存,检测,消毒处理等各环节支持。相信jing准可靠的仪器设备及防护消毒产品一定能为这场战役中的检测工作添砖加瓦。Cole-Parmer与你们一起并肩作战!
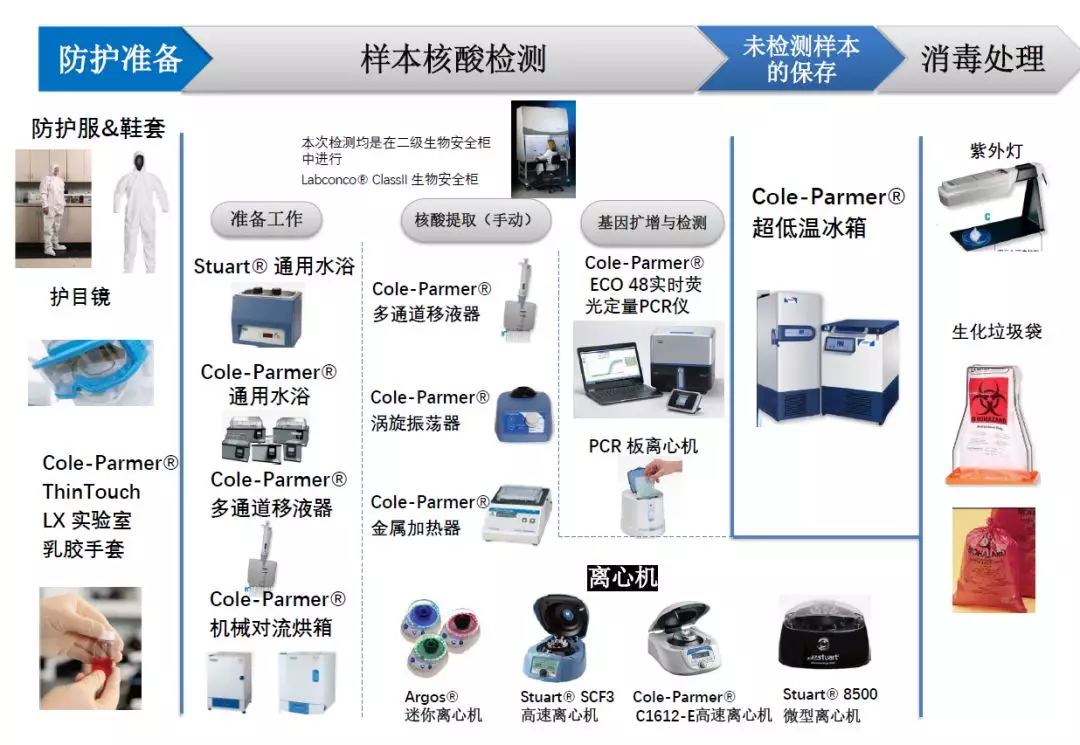
Cole-Parmer相关仪器配置单*手套还有病毒防护丁 腈系列可选
以下是新冠病毒核算检测实验的具体标准介绍,可供各位老师参考,其中涉及的仪器设备和耗材,疫情期间欢迎在微信平台直接联系我们,或者直接联系您当地的销售或经销商。
新冠病毒核酸检测实验
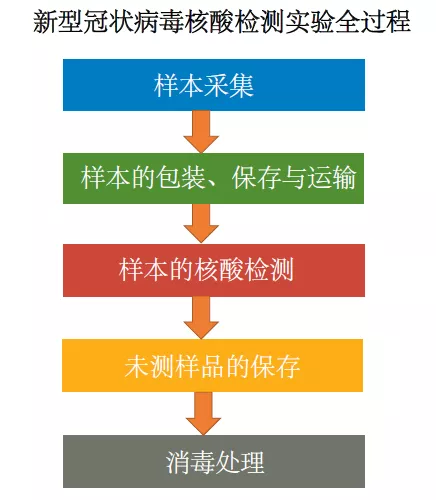
diyi步:样本采集
通常是在采集地——定点发热门诊进行样本选取。样本一般为鼻咽或口咽拭子、气管吸出物、痰液等。鼻咽拭子居多(其阳性率非常高)
在采集过程中,Cole-Parmer可为您提供防护服,护目镜,鞋套,以及手套等防护用品。
第二步、样本的包装、保存与运输
通常采样管需经过3层包装,即:自封袋+运输罐+专用运输箱。在2-4℃进行保存,(通常保存不能超过72小时),再通过UN2814感染性物质专用运输箱,由经过生物安全培训的专人,全身着防护用品运送转运箱。
第三步、样本的核酸检测
实验地点:基因扩增实验室
实验条件:二级生物安全实验室(P2负压实验室)
防护准备:检测人员需进行三级防护的穿戴。按序依次穿戴好一次性帽子、医用N95口罩、一次性防护服、一次性鞋套、一次性防水靴套、护目镜和双层乳胶手套。如有条件可加穿一次性隔离衣。
检测步骤:准备工作,核酸提取(手动),基因扩增与检测,结果分析
1.准备工作
实验仪器设备:二级生物安全柜,水浴或烘箱,移液器
首先检查运输罐是否严格密闭,然后取出罐内的密封袋进行56℃下30分钟的消毒灭活,灭活后可从密封袋内取出采样管对采集的样品进行分装、混匀。
整个过程应在二级生物安全柜内进行,灭活设备应尽量选择可放置于生物安全柜内的小型设备以减少样品进出安全柜内的次数。
2.核酸提取(手动)
实验仪器设备:二级生物安全柜,移液器,振荡器,金属加热器,微型离心机
首先需要依据不同品牌试剂盒的要求进行裂解液的配置。然后,采用化学试剂法对核酸样本进行裂解,样品裂解前需经过充分的振荡混匀,如有必要可采用金属加热器于56℃下充分裂解病毒所释放出的核酸。通过多次离心完成裂解产物的过滤收集。Z后利用离心纯化法对裂解后的核酸进行洗涤与回收。
3.基因扩增与检测
实验仪器设备:生物安全柜,PCR板离心机,实时荧光定量PCR仪
首先,需根据不同品牌试剂盒的要求将试剂盒内的不同组分(引物,dNTP,聚合酶等)按各自所需的体积量进行配置,并充分离心混匀。然后将核酸样本依次加入至每个PCR反应管中,加盖密闭后进行充分的混匀、离心。Z后,将PCR反应管置于实时荧光定量PCR仪中,按照试剂盒说明书的要求进行扩增参数的设置后即开始检测。
4.结果分析
Z后,通过计算出的CT值,依据检测试剂盒厂家说明书的判断标准进行判定,阳性、阴性或者不确定。
第四步、未测样品的保存
如样本未能及时检测,需将样本于-70℃或以下进行保存。Cole-parmer专为您提供保存样品的Cole-parmer超低温冰箱。
第五步、消毒处理
生物安全柜内:对台面、仪器、外层手套进行消毒,相关垃圾投入专用YL垃圾桶中。并开启紫外灯照射生物安全柜,时长应不低于30分钟。
核酸检测实验室内:对实验室台面、地面进行消毒,并开启紫外照射灯进行空间消毒,时长应不低于30分钟。
实验人员:按自上而下、由内而外的顺序依次摘脱三级防护穿戴,并置于专用YL垃圾桶内。
YL垃圾:所有与新型冠状病毒相关的YL垃圾需经过湿热高压灭菌(121℃,30分钟)后再作为普通的YL垃圾处理,且垃圾袋上应标注新型冠状病毒YL垃圾的相关信息。
注意:实验试剂、设备等需取得YL器械注册证,科学研究除外。

 扒开新型冠状病毒的外衣
扒开新型冠状病毒的外衣

 评论
评论