1)膜蛋白的结构形成过程研究
成孔毒素(Pore-forming toxin, PFT)能在靶细胞膜上寡聚化形成穿膜通道, 破坏细胞膜结构并使其渗透性增强而导致细胞渗透性溶解。 PFT寡聚体在细胞膜上可以连接形成密排六方结构(hcp)。
Lysenin是来源于蚯蚓的一种PFT,可在鞘磷脂/胆固醇(SM/chol)双层膜结构中寡聚化并形成hcp。实验中,研究人员使用了日本RIBM的超高速视频级原子力显微镜(HS-AFM),对SM/chol双层膜结构中lysenin寡聚体组装成hcp的动态过程进行了实时成像,发现了hcp结构形成的规律。
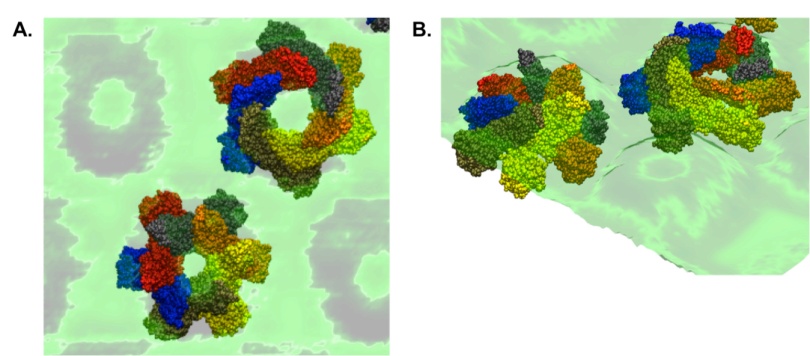
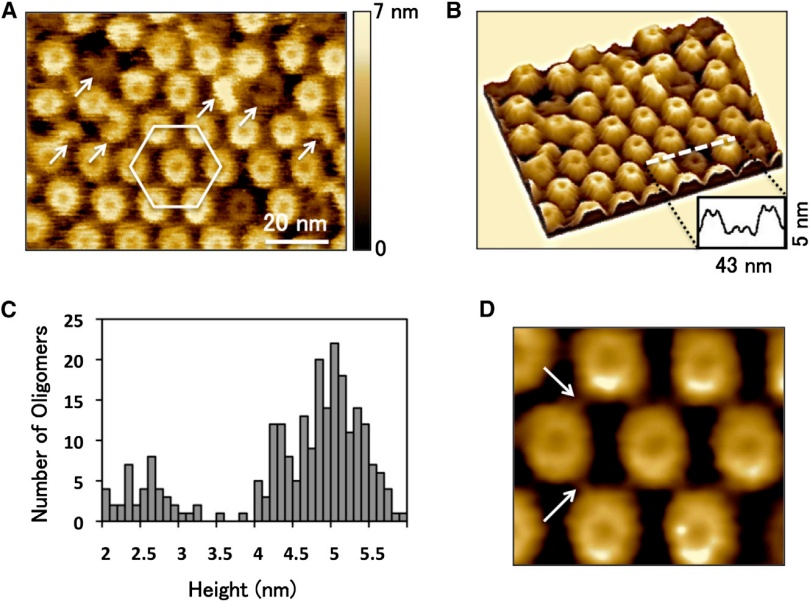
研究人员将lysenin与SM/chol双层膜结构在云母为基底的环境下共同培养后使用HS-AFM进行成像。下图显示了lysenin寡聚体形成的hcp在膜结构上的分布。白色六边形表示一个hcp单元,箭头表示未完全形成的寡聚体。通过计算可以获得Hcp单元的间距和寡聚体直径等数据,与之前使用电镜的研究获得的数据一致。
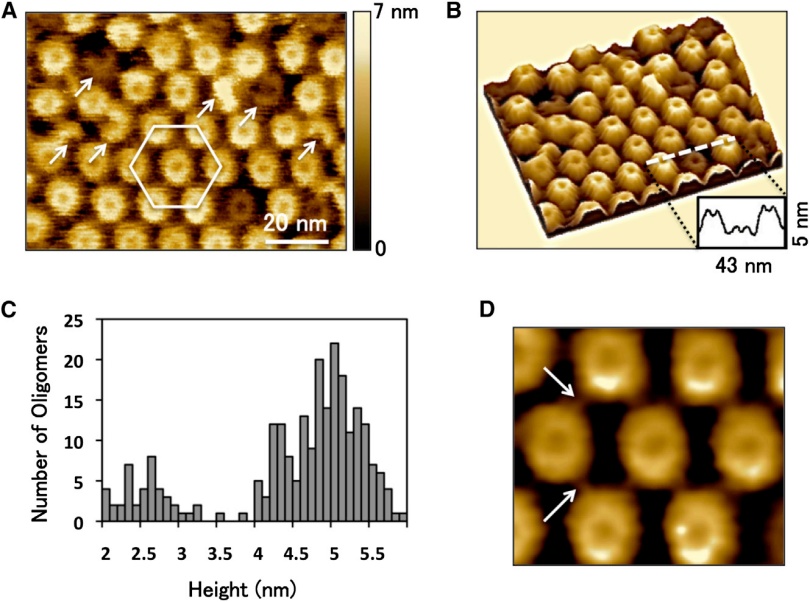
通过HS-AFM还可以获得lysenin寡聚体的三维图像。对各个寡聚体的高度数据进行统计,可以发现高度分布主要为两种,高度较低的寡聚体已经嵌入了膜结构中,并可能形成了核孔。
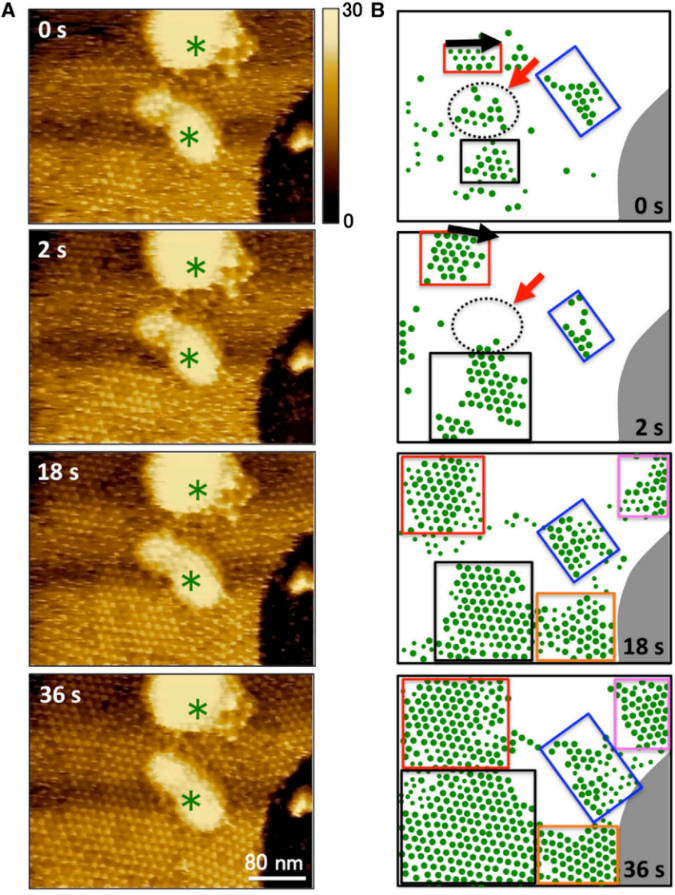
接下来研究人员对400×300nm区域内的SM/chol双层膜结构上的lysenin组装过程进行了动态成像。图A展示了lysenin簇的形成并可以检测簇的增长方向(图B),Z终组装形成hcp结构。
在黑色的云母基底上也能观察到lysenin,分析双层膜结构上和基底上的lysenin半径大小可以得出,双层膜结构上的lysenin形成了寡聚体进而组成hcp结构,而基底上的lysenin处于单体或不规则聚集形态,无法形成寡聚体,这也与之前的研究结果一致。
对视野内的lysenin簇如B图进行划分并进一步分析可以得出:
1. Lysenin形成单个簇后,在双层膜上水平扩散,聚集排列形成hcp结构;
2. 新形成的簇会组成新的矩形排列(彩色矩形)或填充到已有的矩形排列的空缺处,有些已经形成的簇会在膜上扩散或分解;
3. 矩形排列的方向可变(如Z上方红色矩形);
4. 绝大多数Lysenin簇在装配开始就会聚集形成簇,而不是随机分布在膜上。
HS-AFM还可以在更高的放大倍数下以更高速率成像,以实现对lysenin簇组装成hcp结构的动态进行更详细的检测。
通过对结果的分析可以得出,大部分从外围结合到hcp结构区域的簇会以平均0.45秒的时间分解,而已经形成hcp结构的则相对更加稳定,可能原因是内部的lysenin寡聚体相互之间具有更多的结合位点,更难以分解。
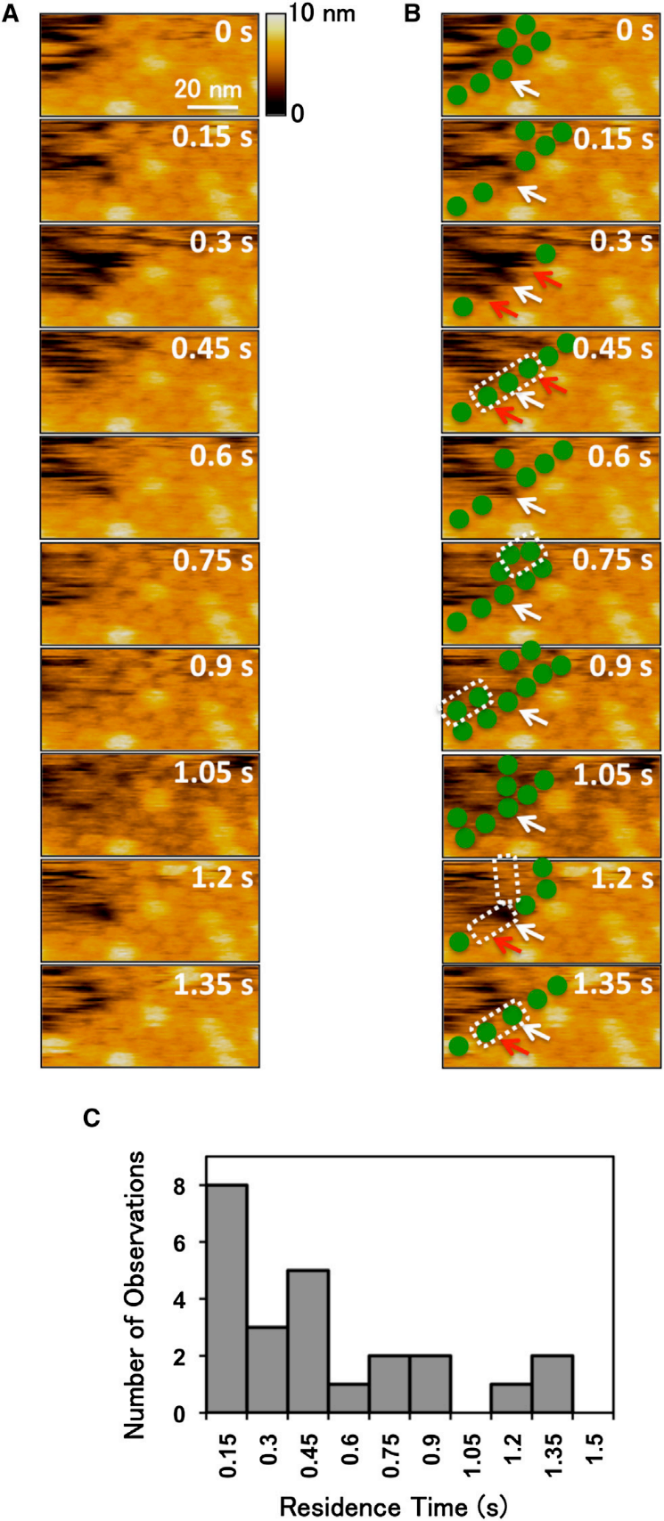
小结:高速AFM成像可用于lysenin形成hcp结构的动态过程的研究。lysenin簇于膜上形成,经过大量的分解\重组和扩散形成hcp结构,随着膜上hcp数量的增多而趋向于稳定。同时,我们还可以获得簇的高度信息,用于表征lysenin与膜的结合以及穿膜通道的形成。
2)膜蛋白的结构形成机制研究
膜联蛋白(Annexin)是于真核细胞的细胞质内普遍存在的一种蛋白,与多种细胞膜功能相关,如胞吞、胞吐以及离子转运等。膜联蛋白在钙离子环境下可结合至磷脂,进行细胞膜修复等作用,但至今对于膜联蛋白-钙离子-磷脂三者的组装与分解的动态过程的研究仍处于空白。
这项研究中,研究人员使用日本RIBM的超高速视频级原子力显微镜(HS-AFM)引导了膜联蛋白V(A5)的组装与分解并进行成像,分析了过程中的蛋白结构,动力学和分子间相互作用。
研究人员首先将双层脂膜加入含2mM钙离子的缓冲液,再加入A5并用HS-AFM成像。可以观察到A5三聚体在膜上形成了六边形晶格结构(标记1),并在中间含有纵向高度更低的三聚体(标记2)或者空洞(标记3),这与先前使用其他AFM和电镜的结果相一致。

HS-AFM可以进行每秒几十帧的更高速度的成像。对上图中标记2的区域进行高速成像,三聚体依然保持了相似的尺寸和高度。在高速成像下,研究人员首次发现三聚体的方向会发生变化:向上(0°)和向下(60°)。此A5三聚体与其他形成了六边形晶格结构的三聚体相比,分子间相互作用更弱,使其能够改变方向。

传统的AFM和电镜获得的图像是时间或空间的平均图像,无法记录极短时间内的变化,因此难以发现三聚体方向的改变。通过HS-AFM的高速实时成像才发现并捕捉到了这一现象。
HS-AFM还可以与微流系统和激光等其他仪器结合,在实验过程中对样品和环境进行更多操作并实时成像,可以对两种A5三聚体的组装与分解进行更加深入、详细的研究。
研究人员使用微流系统可向实验环境加入EDTA,可以降低钙离子含量,使三聚体形成的晶格结构分解,同时,通过精确控制的流量可以jing准地计算出加入EDTA的含量进行定量分析;整合的高精度紫外激光,可以对钙离子笼锁化合物进行解笼锁操作,使其在实验过程中可以多次反复释放钙离子。

起初,我们可以清晰地观察到晶格结构;277s时缓慢加入40mM EDTA后,晶格结构分解;441s时启动紫外激光,解笼锁发生释放出钙离子,晶格结构重新组装;870s时关闭激光,晶格结构再次开始分解。
进一步提高放大倍数后进行高分辨率成像,可以发现加入EDTA后,非六边形晶格的A5三聚体相对于形成了六边形晶格结构的三聚体分解更快,对于钙离子含量下降更加敏感。

小结:通过HS-AFM的高速、高分辨率成像以及与其他仪器的联用,在体外构建了实时生化反应环境,在对蛋白结构直接成像的同时,发现了构成膜联蛋白结构的两种不同状态的蛋白三聚体的差异,同时证明了钙离子在蛋白组装过程中的必要性。
3)膜蛋白的跨膜运动机制研究
谷氨酸盐跨膜转运蛋白(GltPh)的主要作用是通过跨膜转运谷氨酸盐,将突触间隙的谷氨酸盐浓度保持在兴奋性毒性以下,防止神经元死亡导致神经系统疾病如癫痫、老年痴呆等。
GltPh如右图所示,由一个固定在膜上的三聚体结构域(橙色)和一个转运结构域(蓝色)组成。在有钠离子和谷氨酸的环境下,转运结构域可移动至膜的对侧来转运谷氨酸盐;在无基底的环境下,转运结构域也可以跨膜移动。
之前,GltPh的直接动态成像很难实现,RIBM的超高速视频级原子力显微镜(HS-AFM)攻克了这一难关,向我们展示了GltPh的跨膜升降运动。
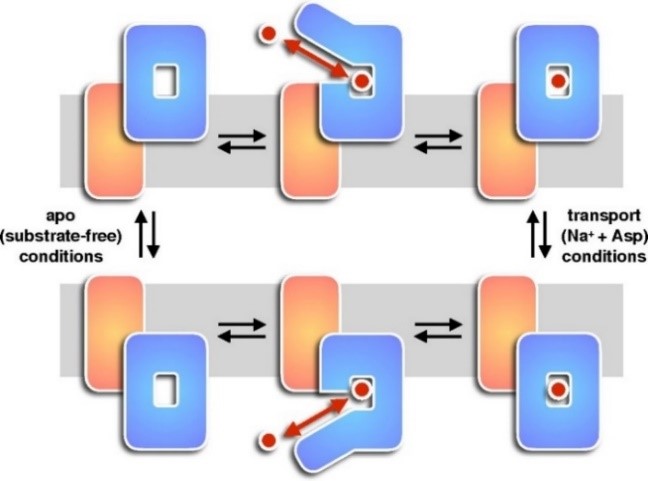
实验开始前,研究人员将GltPh纯化后与脂类组成的囊泡整合成跨膜结构,并用HS-AFM观察。
在无基底的环境下,GltPh的三聚体结构清晰可见。当每个转运结构域暴露在胞外的部分朝向显微镜的探针,即处于上升(up)状态,突出的部分形成了一个三角形,中间则形成空洞(t=57s);每个转运结构域也可朝向胞内(t=58s),此时处于下降(down)状态。


环境中单独加入钠盐时,GltPh处于上升状态的平均时间为33s,这意味着GltPh仅结合Na+离子时跨膜运动受到YZ。
加入充足的钠盐和谷氨酸,使环境浓度达到饱和后,GltPh处于上升状态的平均时间为 11.1 s,开始进行活跃的跨膜转运活动。
以上的结果证实了,当Na+和谷氨酸同时存在或缺失时,GltPh的跨膜运动相对于仅有Na+时更加活跃,GltPh是Na+和谷氨酸的协同转运载体。

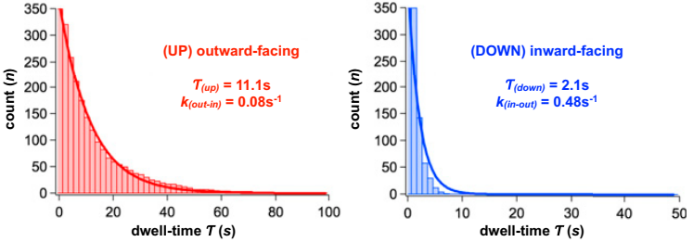
HS-AFM在进行高速成像的同时,保持了很高的空间分辨率,可以清晰地分辨三聚体的每一个结构域,使得我们可以对不同结构域运动之间的关系进行研究。
我们针对一个GltPh三聚体,通过视频统计的数据计算了其处于不同状态(结构域处于上升状态的数量)的概率,结果与使用自由能公式计算出来的概率一致。
进一步对结构域运动的关系进行统计,可以得出三聚体的结构域之间运动是相互独立的,这也直接验证了之前的研究结果。
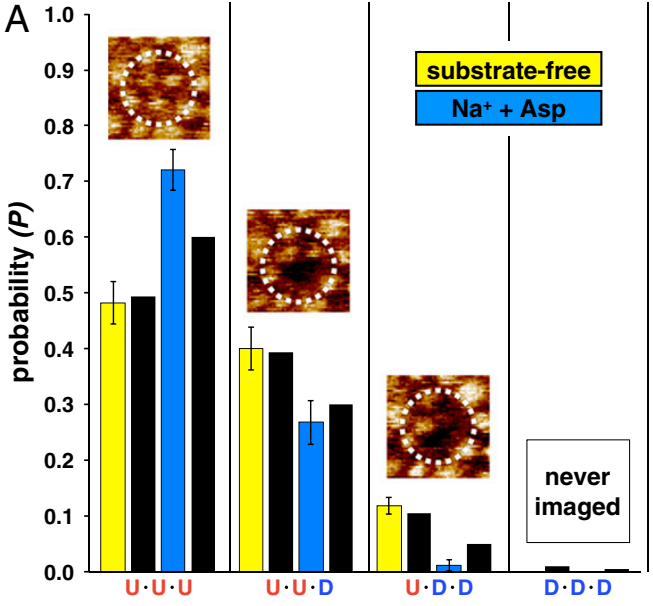
小结:使用HS-AFM获得的高空间&时间分辨率的视频级图像,可以准确地反应生物大分子的运动状态,用于精确定量研究。

 评论
评论