发布:
安捷伦科技(中国)有限公司时间:
2022-11-25行业:
医疗卫生 医院在药物研发中,药效是研究者S要关注的对象,但是随着药物研发的进行,安全性更应该成为药物研发中Z需要考虑的因素。据统计,2015年中止的药物临床项目中就有超过50%的药物是因为安全性问题。
其中心脏毒性一直是药品召回和FDA黑框警告(Black Box Warnings, 是美国 FDA 对上市药物采取的一种Z严重的警告形式,要求在药品说明书Z靠前、Z醒目的位置添加粗加黑的方框,对药物的使用风险进行提醒)的主要原因。抗肿瘤药物心脏毒性是指在使用某些抗肿瘤药物对癌症患者进行治 疗后,药物对患者心肌和/或心电传导系统产生毒性作用,从而引起的心脏病变。在2020年FDA就因心脏毒性原因召回27种药品。在2021年FDA更新3款JAK抑 制剂药物的黑框警告,警告用药会增加患者心脏病和中风等心脏疾病的风险。
近年来,生物药和小分子等抗肿瘤药物研发数量激增,因此为了确保药物的临床安全,研发人员有必要将药物诱导的心肌毒性或者off-target效应在临床申报前完成验证。安捷伦细胞分析事业部在药物心脏安全性评估方面可以提供全面的工具支持。
人诱导干细胞来源的心肌细胞(hiPSC-CM)的诱导分化
心肌细胞不具备自我更新能力,体外心脏毒性检测需在人诱导干细胞来源的心肌细胞,Agilent xCELLigence RTCA ePacer为获得功能成熟的 hiPSC-CM提供了一种简便有效的方法。在精确、一致的电刺激条件下,ePacer在2–3周内即可改善hiPSC心肌细胞的成熟状态,并且不会对细胞产生任何可检测到的毒性或应激。可同时刺激多达6块E-Plate中的细胞,以进行更多高通量实验。

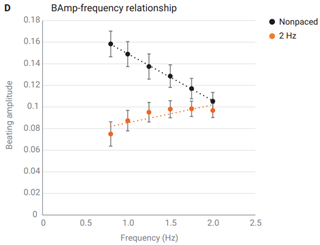
使用幅度/频率关系和内置算法评估心肌细胞成熟度
药物诱导的心肌细胞收缩和离子通道损伤评估
hIPSC-CM诱导成熟后使用 xCELLigence RTCA CardioECR 系统评估同一块板子中hiPSC-CM在药物诱导后的的收缩反应,离子通道(Na+, Ca2+, 及 K+)活性和心肌细胞活力等。
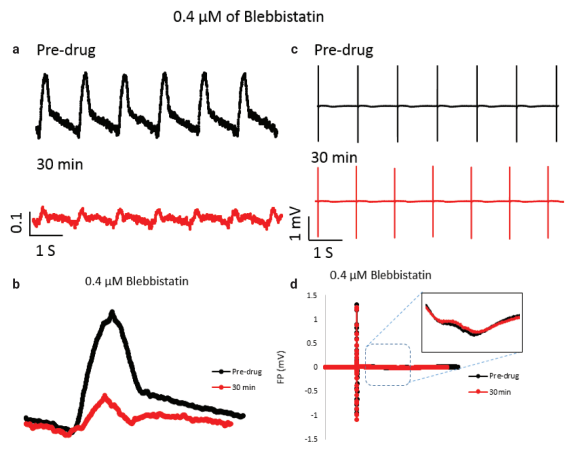
评估hiPSC心肌细胞的收缩反应和电反应
通过成像对心肌细胞数量以及活率分析
hIPSC-CM诱导成熟后,在E-Plate Cardio VIEW 96 上使用 Agilent xCELLigence RTCA eSight系统对细胞进行成像采集,通过成像数据分析孔内的细胞数量,或者通过死细胞染料和阻抗检测心肌细胞在药物诱导下的活率变化。

Agilent xCELLigence RTCA eSight
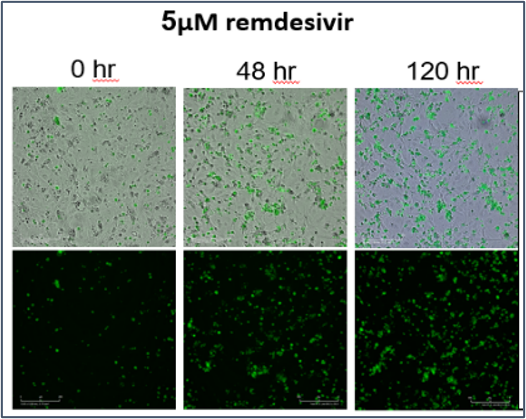
抗病毒 药物瑞德西韦对hiPSC-CMs毒性(绿色为AnneixnV)
心肌细胞线粒体毒性分析
线粒体对于维持心肌细胞正常功能具有至关重要的作用,线粒体结构与功能异常会导致心肌病的发生与发展。Agilent Seahorse XFe96分析仪以微孔板形式测定心肌细胞在药物诱导下的线粒体呼吸和糖酵解的改变。另外,也可以直接利用Agilent MitoXpress Xtra试剂以高通量形式来确定呼吸速率以进行心肌细胞代谢表征并评估药物对线粒体功能毒性作用。

Agilent seahorse XFe96 Analyzer
Agilent MitoXpress Xtra试剂
小结
安捷伦提供行业领先的集成工作流程解决方案,实时评估药物引起的心脏毒性,可应用于化药,小分子靶向药,抗体药以及细胞治疗药物等。安捷伦的解决方案可生成更全面的数据,包括心肌细胞的收缩,电生理,活力,糖酵解,耗氧率以及线粒体毒性等,提高评估药物诱导性心脏毒性的数据质量。想要了解更多实验步骤,请点击下图,了解更多……
