发布:
北京莱伯泰科仪器股份有限公司时间:
2021-05-08行业:
制药/化妆品 中药近年来,随着医药产业的快速发展和公众对药品安全认知水平的不断提升,加强对中药外源性有害物质的控制,建立有关标准已成为满足药品监管需求、保障公众用药安全的重要手段。中药材大部分来源于植物和动物,在种植(养殖)过程中不可避免地会发生病虫草害,需要使用农药进行FZ;而使用农药不意味着滥用农药,国家对于高毒、高残留、高安全风险的化学农药出台了禁用名单,需要首先加以监控。
在参考了我国农业农村部自2002年至今发布过的化学农药禁限用公告后,《ZG药典》2020年版经剔除杀鼠剂、重金属类农药、熏蒸剂、多异构体、难以获得对照品及难以采用常规气质、液质测定的农药品种后,总计 33 种农药 55 个化学单体作为禁用农药检测品种的检测指标。
本文参考2020版《ZG药典》2341 通则中的第五法使用LabTech SPE 1000全自动固相萃取系统对常用根茎类药材甘草中的农药进行固相萃取,分别采用GC-MS、LC-MS检测,建立了一套中药农残的处理检测方法,其中GC-MS组分别采用GCB/NH2柱净化与HLB柱净化样品,两种方法的回收率及平行性良好,加标回收率分别为71.1%~101.2%和73.3%~106.7%,重复性RSD分别为1.2%~8.6%和1.3%~9.0%,LC-MS组采用HLB柱净化样品,加标回收率为74.8%~113.4%,重复性RSD为2.3%~9.8%,均满足药典要求,适合2341第五法通则所规定中药农残检测。
1 仪器设备及试剂
1.1仪器设备
SPE 1000全自动固相萃取系统(莱伯泰科公司);7890B-5977B气相色谱质谱联用仪(安捷伦公司);SCIEX Exion LC™液相系统+ Triple Quad™ 4500质谱系统(SCIEXZG公司);MultiVap-10全自动高通量平行浓缩仪(莱伯泰科公司);EV400VAC旋转蒸发仪(莱伯泰科公司)。


1.2 试剂及耗材
乙腈(色谱级);甲苯(农残级);乙腈-甲苯混合溶液(3∶1),现用现配;氯化钠(分析纯);蒸馏水;HLB固相萃取住(200mg,6mL,莱伯泰科);GCB/NH2固相萃取柱(500mg/500mg,6mL,莱伯泰科)33种农残混标工作液:5μg/L,溶剂为乙腈,购自坛墨质检;磷酸三苯酯内标工作液:0.1mg/L,溶剂为乙腈,购自坛墨质检;30种农残混标工作液:5μg/L,溶剂为乙腈,购自坛墨质检。
2 实验方法
2.1 样品处理
称取甘草粉末(过3号筛)5g,加氯化钠1g,摇散后加入乙腈50mL,匀浆处理2min(每分钟不低于12000转),离心5min(每分钟4000转),取上清液,沉淀再加入50mL乙腈匀浆,离心,合并两次上清液,旋蒸浓缩至3~5mL后,用乙腈定容至10mL。
2.2 GCB/NH2柱固相萃取法
将2.1制得的样品各取2mL放入SPE 1000全自动固相萃取系统,按照图1所示的方法进行样品的固相萃取净化步骤。收集洗脱液,旋蒸浓缩,用乙腈转移并定容至2mL。
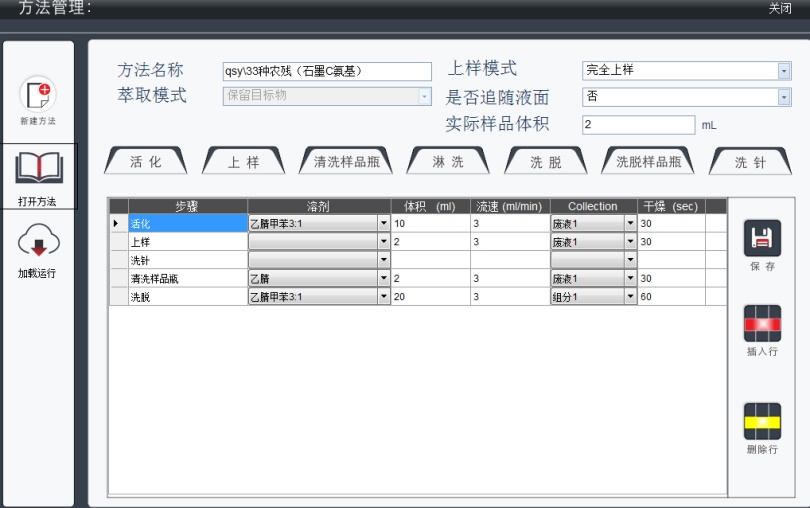
图1 GCB/NH2柱固相萃取流程
2.3 HLB柱固相萃取法
将2.1样品各取3mL放入SPE1000全自动固相萃取系统,按照图2所示的方法进行样品的固相萃取净化步骤,收集净化液。

图2 HLB柱固相萃取流程
2.4 基质加标回收率实验
基质标准曲线的配制:分别按照2.2、2.3制备空白基质溶液,各取1mL(每种方法所得样品平行6份)至MultiVap-10全自动高通量平行浓缩仪上,40℃浓缩至约0.6mL,分别加入10μL、20μL、50μL、100μL、150μL、200μL混标工作液,加乙腈定容至1mL,混匀。
按2.1方法准备样品,进行加标实验,5g样品加标1μg,然后分别按照2.2、2.3方法进行实验,同时进行6个平行样品,用来测定加标回收率及平行性。
取处理好的样品溶液(或基质混标溶液)1mL,GC-MS法精密加入内标0.3mL,LC-MS法精密加入水0.3mL,混匀待测。
2.5 GC-MS分析条件
2.5.1 气相色谱条件
色谱柱:Agilent DB-5ms毛细管柱:30 m*250 μm*0.25μm;
进样口温度:270℃;
柱温程序:初始温度100℃,以5℃/min升至180℃,保持5min,然后以5℃/min升至220℃保持6min,再以10℃/min升至280℃,保持5min。
进样量:1 μL;
进样方式:不分流进样;
流速:1.0mL/min;
2.5.2 质谱条件
离子源温度:280℃;
辅助加热温度:290℃;
溶剂延迟:3min;
扫描方式:全扫描(SCAN)方式用于定性/选择离子扫描模式(SIM)用于定量。
2.6 LC-MS分析条件
2.6.1 液相色谱条件
色谱柱:Shim-pack Velox C18(2.7μm,2.1*100mm);
流动相:A: 0.1%甲酸溶液(含5 mmol/L 乙酸铵);B:乙腈-0.1%甲酸溶液(含5 mmol/L乙酸铵)(95:5);
流速:0.4 mL/ min;柱温:40℃;进样量:2 μL;
洗脱梯度:0~1min,30%B;7min~8min,100%B;8.1~10min,30%B。
2.6.2 质谱条件
离子源:ESI源,正离子模式;
离子源参数:
IS电压:5500V 气帘气CUR:30 psi;
雾化气GS1:55 psi 辅助气GS2:55 psi;
源温度TEM:550℃碰撞气CAD:Medium。
3 结果和讨论
3.1 各样品色谱图
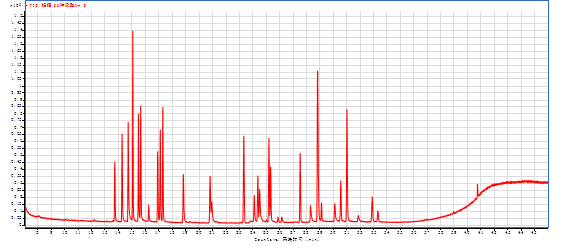
图3 标准工作液GC-MS总离子流色谱
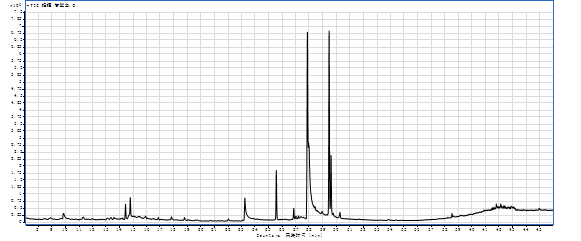
图4 空白样品GC-MS总离子流色谱图
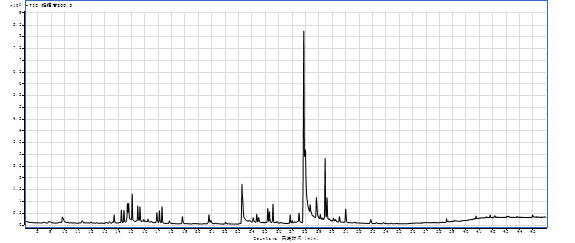
图5 基质加标GC-MS总离子流色谱图
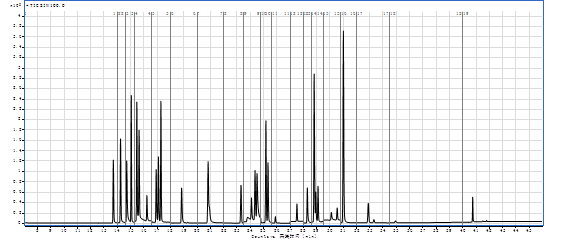
图6 标准工作液GC-MS选择离子流色谱图
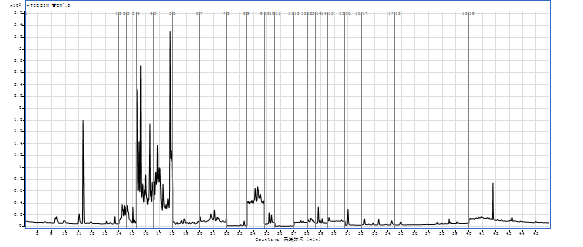
图7 基质加标GC-MS选择离子流色谱图
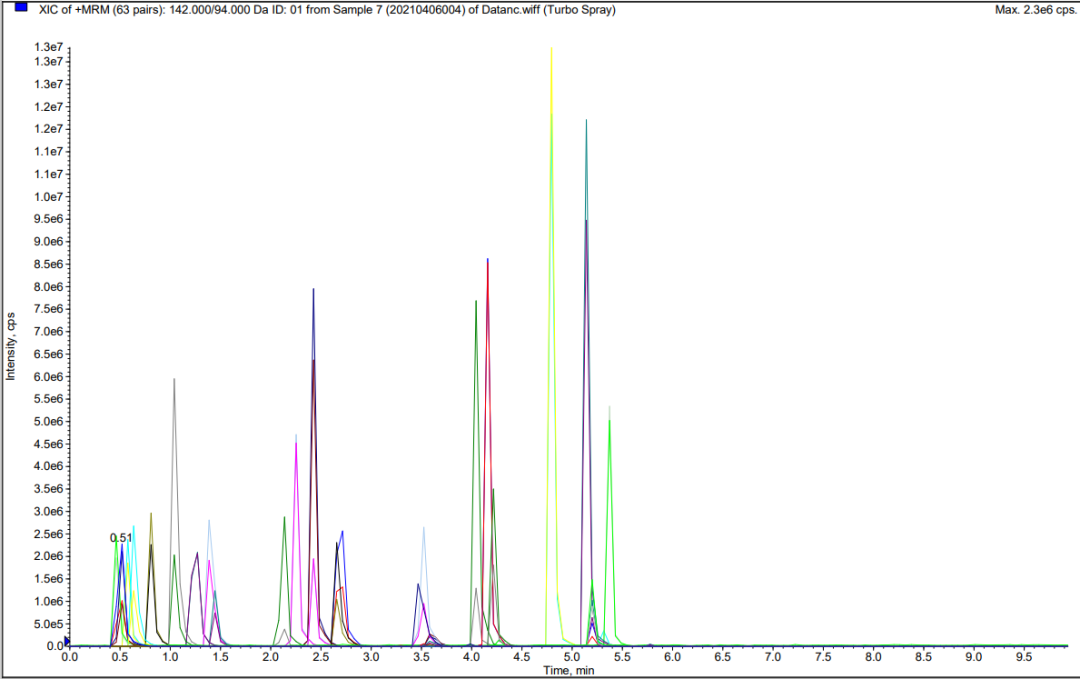
图8 标准工作液LC-MS总离子流色谱图
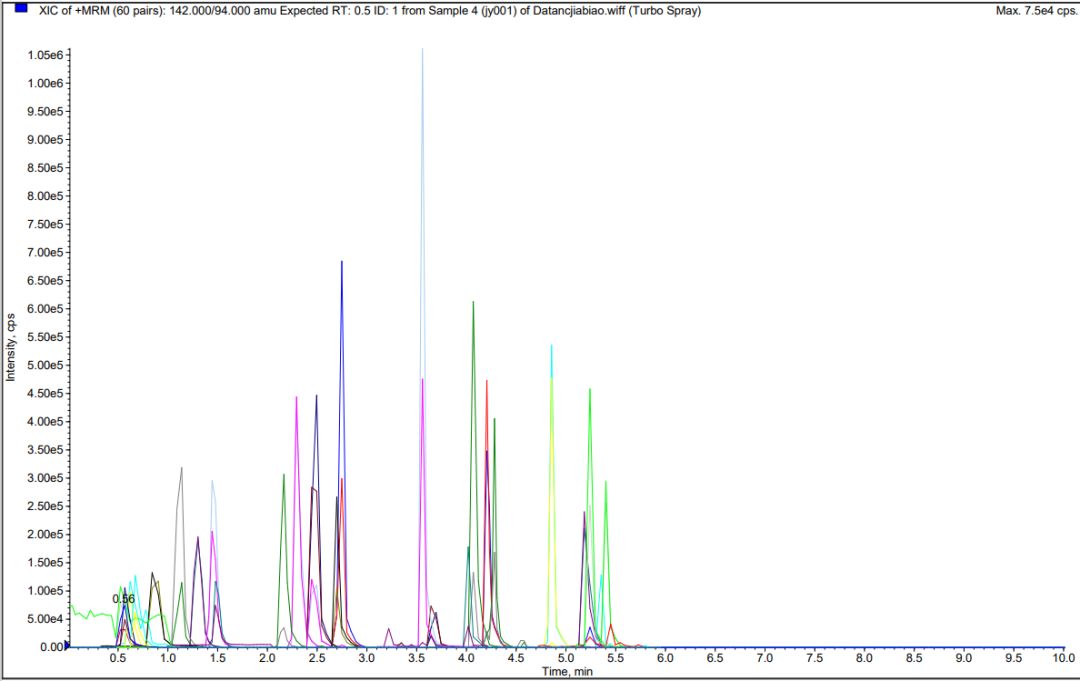
图9 基质加标LC-MS总离子流色谱图
3.2 标准曲线
按2.4中的配制的基质混标溶液(0.05μg/mL~1μg/mL)计算得出各组分(以相对峰面积和相对浓度作标准曲线) 的线性方程、相关系数,见表1、2、3。
表1 33种农残GC-MS法线性方程(GCB/NH2柱固相萃取法)
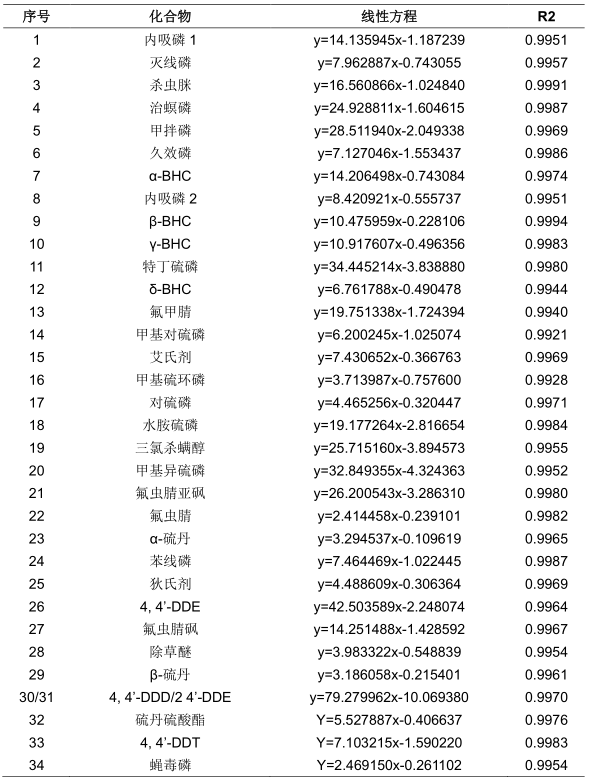
表2 33种农残GC-MS法线性方程(HLB柱固相萃取法)
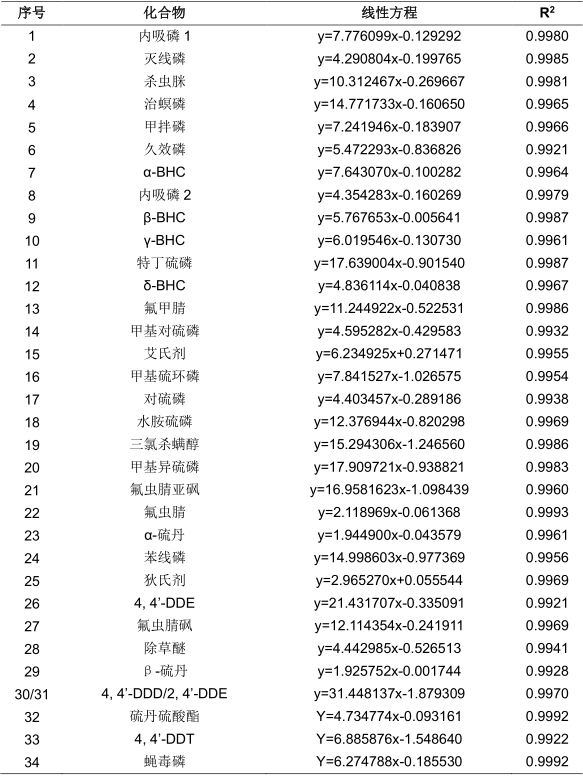
表3 30种农残LC-MS法线性方程(HLB柱固相萃取法)

3.3 加标回收率
加标样品经固相萃取净化、洗脱、浓缩后,分别进行GC-MS、LC-MS分析,定量,计算得到的加标回收率及相对标准偏差如表4、5、6所示。
表4 33种农残GC-MS法加标回收率(GCB/NH2柱固相萃取法)
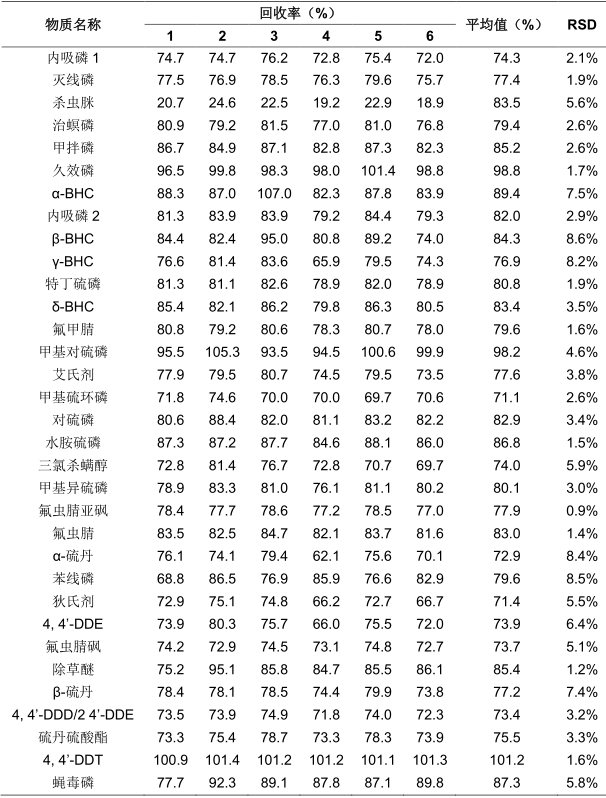
表5 33种农残GC-MS法加标回收率(HLB柱固相萃取法)
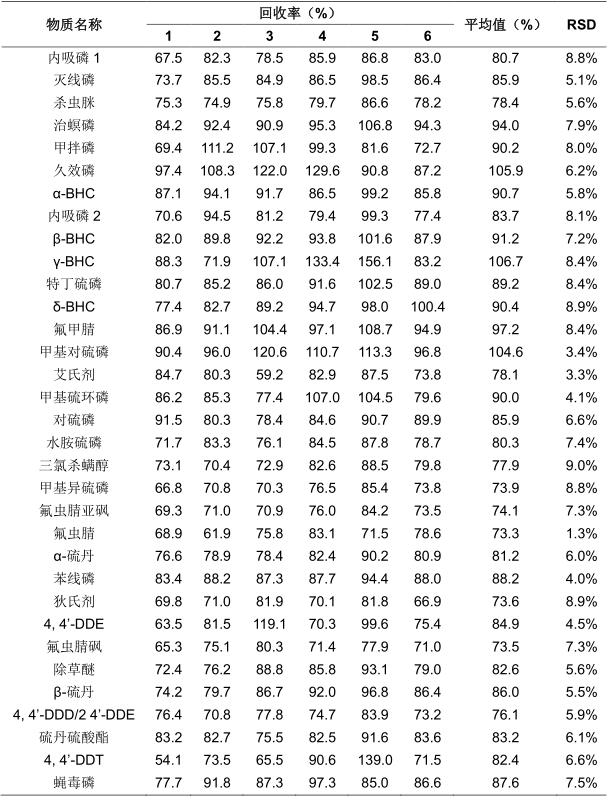
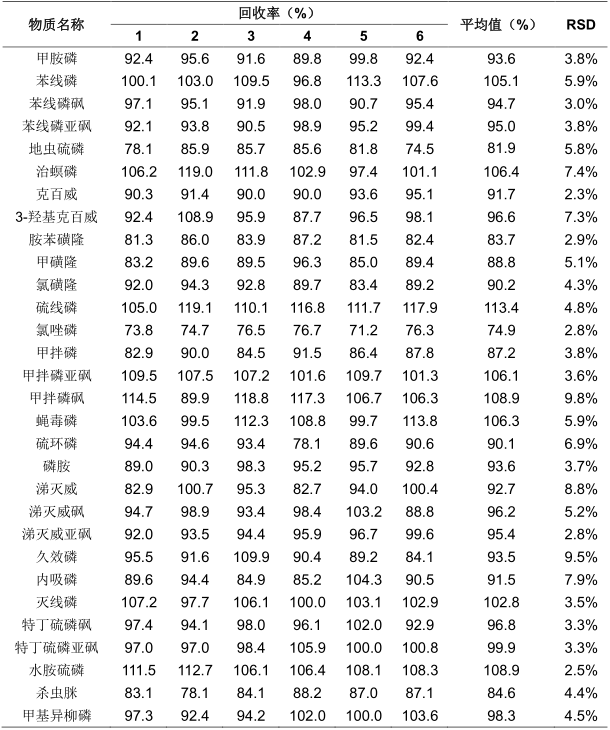
表6 30种农残LC-MS法加标回收率(HLB柱固相萃取法)
4 实验结论
由表4、5、6可知,2020版《ZG药典》2341第五法GC-MS组中GCB/NH2柱固相萃取和HLB柱固相萃取的加标回收率分别为71.1%~101.2%和73.3%~106.7%,重复性RSD分别为1.2%~8.6%和1.3%~9.0%,LC-MS组HLB柱固相萃取的加标回收率为74.8%~113.4%,重复性RSD为2.3%~9.8%,均满足药典要求。
综上所述,莱伯泰科SPE1000全自动固相萃取系统、EV400VAC旋转蒸发仪及MultiVap-10全自动高通量平行浓缩仪能够gao效、稳定地达到实验的要求,适用于2020版《ZG药典》2341第五法中规定的中药农残测定,适用于中药甘草样品的前处理实验。
5 参考文献
[1] 中华人民共和国药典2020年版. 四部[S].2020: 30ChP 2020. VolⅣ[S]. 2020: 30.
[2] 申明睿,翟为民,何轶,石上梅,杨昭鹏,兰奋.《中华人民共和国药典》2020年版中药禁用农药残留限量标准的研究思路[J].药物分析杂志,2020,40(11):2075-2081.